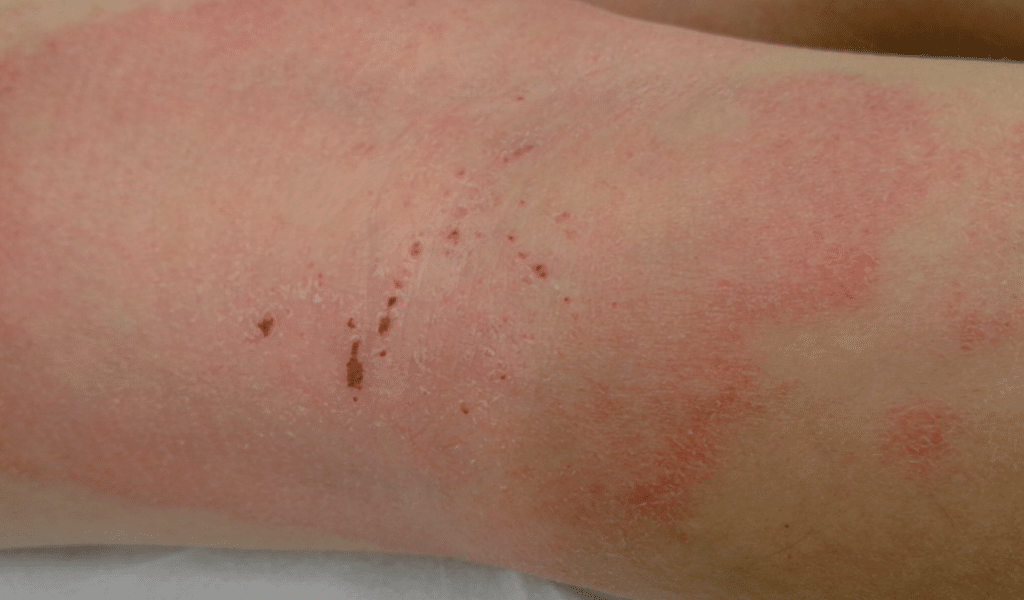
Atopische Dermatitis, Patientenbild aus der Advantage Studie
Unerwünschte Ereignisse führen angesichts der vorliegenden Daten von Paller et al. nur selten dazu, dass Heranwachsende mit mittelschwerer bis schwerer atopischer Dermatitis (AD) die Therapie mit Lebrikizumab beenden.
Die Therapieoptionen bei Heranwachsenden mit AD sind begrenzt. Demgegenüber steht ein hoher medizinischer Bedarf – denn bei einer weltweiten Prävalenz von bis zu 5 % sind bis zu 50 % der Betroffenen dieser Altersgruppe mittelschwer bis schwer erkrankt.
Wirksamkeit und Sicherheit des monoklonalen Anti-Interleukin (IL)-13-Antikörpers Lebrikizumab bei Jugendlichen im Alter von 12 – 18 Jahren sind durch die placebokontrollierten doppelblinden Phase-3-Studien ADvocate 1 & 2 sowie ADhere belegt. In der hier vorgestellten offenen, 52- wöchigen Phase-3-Studie ADore wurde im primären Endpunkt untersucht, wie viele der 206 Patienten im Alter von 12 – 18 Jahren mit mittelschwerer bis schwerer AD die Therapie mit Lebrikizumab 250 mg alle zwei Wochen s.c. (nach 500 mg in Woche 0 und 2) aufgrund unerwünschter Ereignisse bis zur Abschlussvisite beendet haben.
Am Ende der 52-wöchigen Behandlung waren noch 172 der 206 Patienten (83,5 %) unter Lebrikizumab verblieben. Häufigste Gründe für das Absetzen der Medikation waren das Ausscheiden aus der Studie (6,3 %) und Lost to Follow- Up (3,9 %). Insgesamt berichteten 65 % der Patienten über meist mild bis moderat ausgeprägte Nebenwirkungen. Die Häufigkeit schwerer unerwünschter Ereignisse und zum Behandlungsabbruch führender Nebenwirkungen war mit jeweils fünf Patienten (je 2,4 %) gering. Sekundäre Endpunkte waren unter anderem der Anteil an Patienten mit einem EASI-75 und EASI-90, sowie weitere Aspekte die soziale Faktoren wie Lebensqualität, Ängstlichkeit und Depression abbilden.
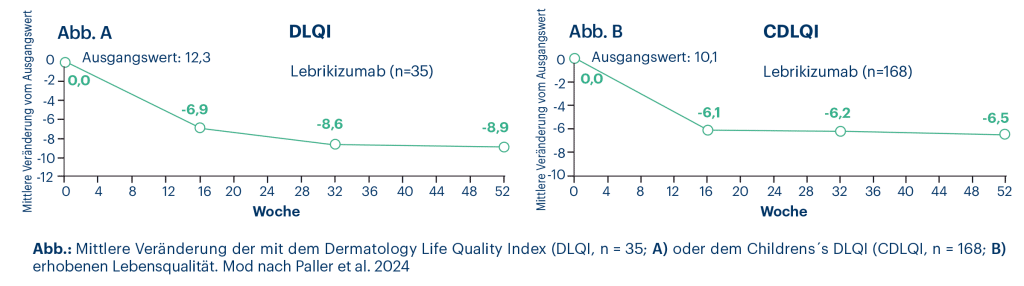
Hinsichtlich der Wirksamkeit zeigten nach vier Wochen 28,6 % der Patienten eine mindestens 75 %ige Verbesserung im Eczema Area and Severity Index (EASI). Der Anteil erhöhte sich auf 73,2 % in Woche 16 und weiter auf 81,9 % in Woche 52. 61,4 % der Patienten erreichten bis Woche 52 ein EASI-90-Ansprechen. Der mittlere Body Surface Area (BSA)-Index sank im Studienverlauf von 45,4 % auf 8,4 % ab. Einschränkungen der mit dem (Children´s) Dermatology Life Quality Index (CDLQI, DLQI) erhobenen Lebensqualität gingen bis Woche 52 um durchschnittlich -6,5 bzw. -8,9 Punkte zurück. Im Patient-Reported Outcomes Measurement Information System (PROMIS) waren die Werte für Angst und Depression von Woche 16 bis 52 gegenüber dem Ausgangswert anhaltend vermindert.
In der offenen Studie zeigte Lebrikizumab bei Heranwachsenden mit mittelschwerer bis schwerer AD über 52 Wochen hinweg ein mit früheren Studien konsistentes Sicherheitsprofil, ziehen die Autoren als Fazit. Bei einer niedrigen Rate an schweren oder zum Therapieabbruch führenden Nebenwirkungen im Studienverlauf setzte schon in den ersten vier Wochen eine Verbesserung des Hautbildes ein.
Quelle: Paller, A.S., et al. (2023). “Safety and Efficacy of Lebrikizumab in Adolescent Patients with Moderate-to-Severe Atopic Dermatitis: A 52-Week, Open-Label, Phase 3 Study.” Dermatol Ther (Heidelb) 13: 1517-1534