First Choice.
So wirkt EBGLYSS®
Wirkmechanismus
Wirksamkeit & Sicherheit
Einfache Anwendung
EBGLYSS® ist in zwei Darreichungsformen erhältlich, als Fertigpen und Fertigspritze:
250 mg
250 mg
Für Ärztinnen und Ärzte
EBGLYSS® überzeugt auch im Praxisalltag:
Erste Ergebnisse aus der NIS ADlife bestätigen frühe & starke Wirksamkeit auf Juckreiz & Hautzustand kombiniert mit einem überzeugenden Sicherheitsprofil.

Ergebnisse der ADvocate 1 & 2 Studien
Die beiden zulassungsrelevanten Monotherapiestudien belegen die Wirksamkeit und Sicherheit von EBGLYSS® (Lebrikizumab) bei mittelschwerer bis schwerer atopischer Dermatitis. Erfahren Sie mehr über Studiendesign, Endpunkte und klinische Relevanz.
Thieme Case Report
Gezielte IL13-Hemmung in der Praxis: Vier Fälle mit Lebrikizumab bei atopischer Dermatitis.
Copyright Georg Thieme Verlag KG 2026

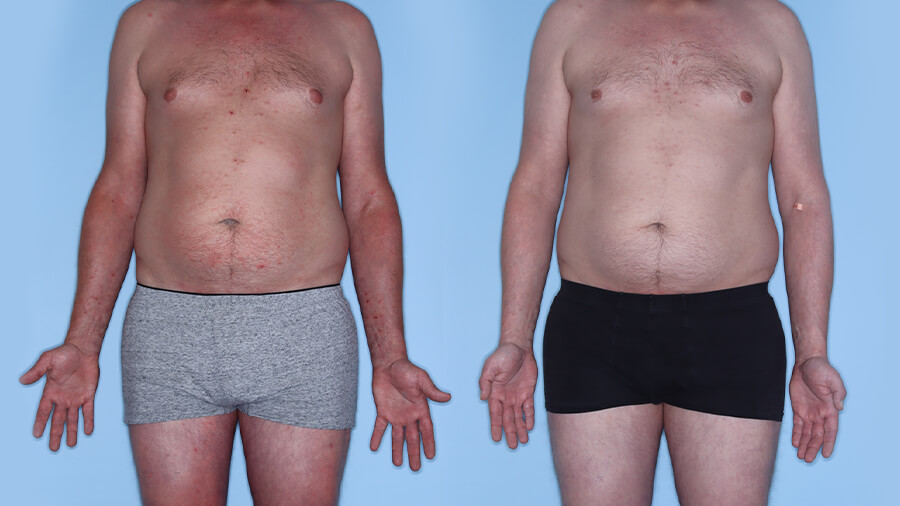
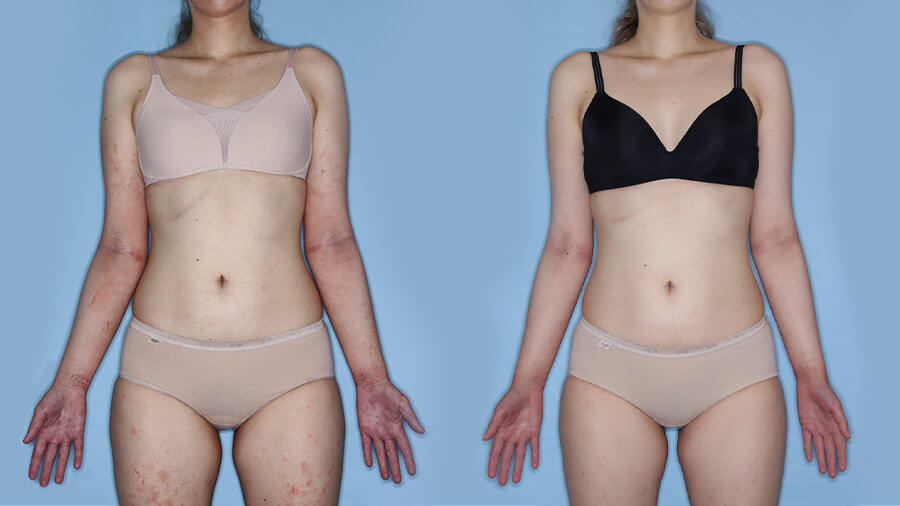
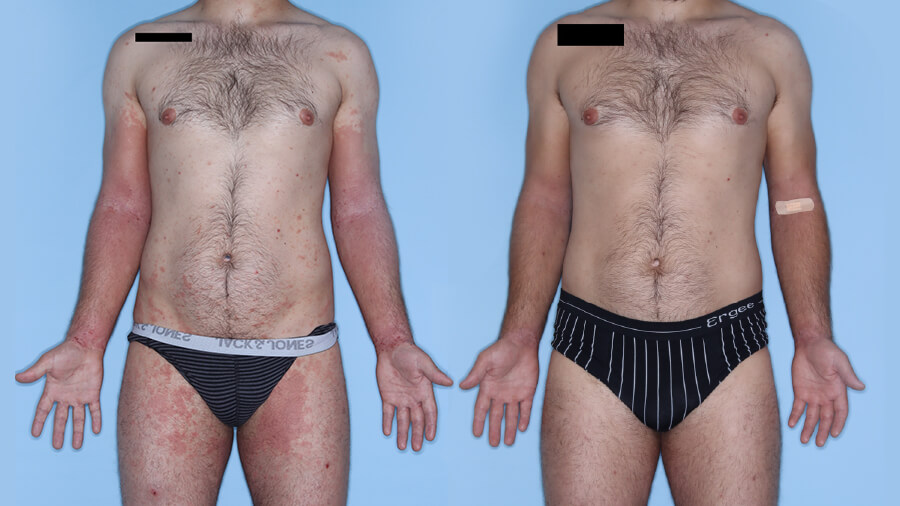
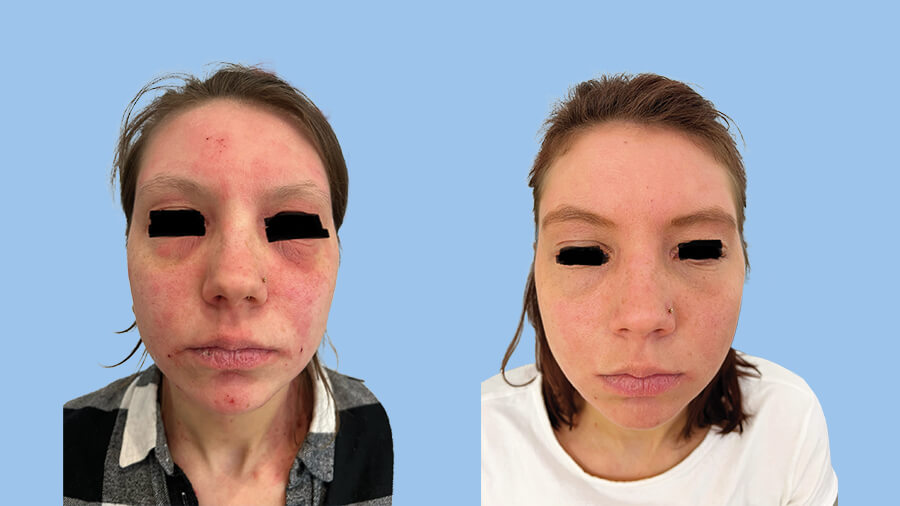
Patientenfälle auf einen Blick
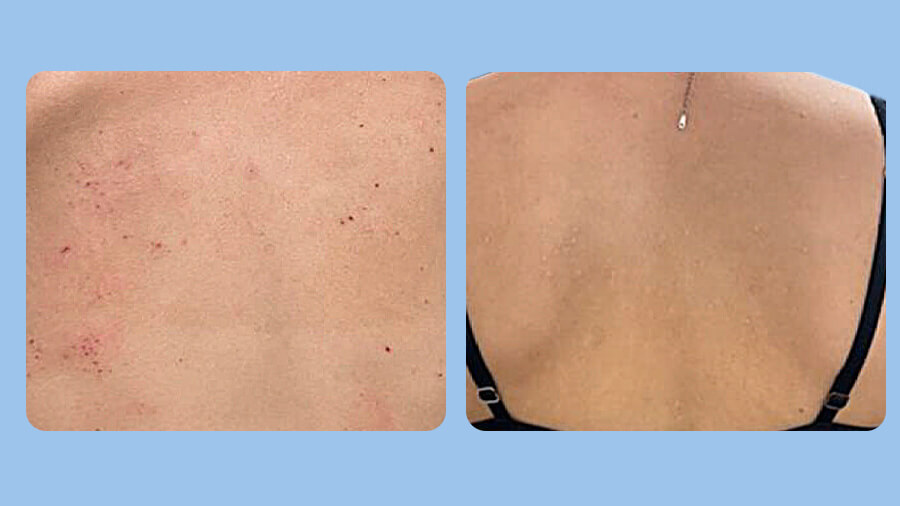
Erfolgreiche Verbesserung Hautzustand & Pruritus bei Patientin mit atopischen Komorbiditäten
Almirall meets...
Dr. Ante Karoglan
In diesen kurzen Experteninterviews erläutert Dr. Ante Karoglan aus Berlin den Einsatz von Lebrikizumab bei mittelschwerer bis schwerer atopischer Dermatitis. Im Fokus stehen Patientenselektion, Real-World-Erfahrungen, Wirksamkeit und Sicherheit sowie der Einfluss auf den oft belastenden Juckreiz.

Servicematerialien
Informationsmaterialien
Für Ihre Patient:innen
Unsere Patientenbroschüre in verschiedenen Sprachen
EBGLYSS® Produktprofil
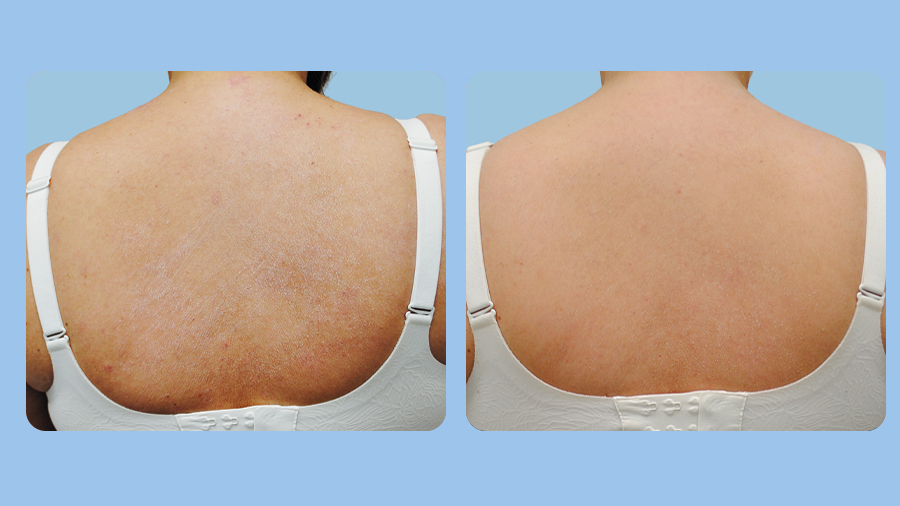
Deutliche Hautverbesserung in der Monotherapie
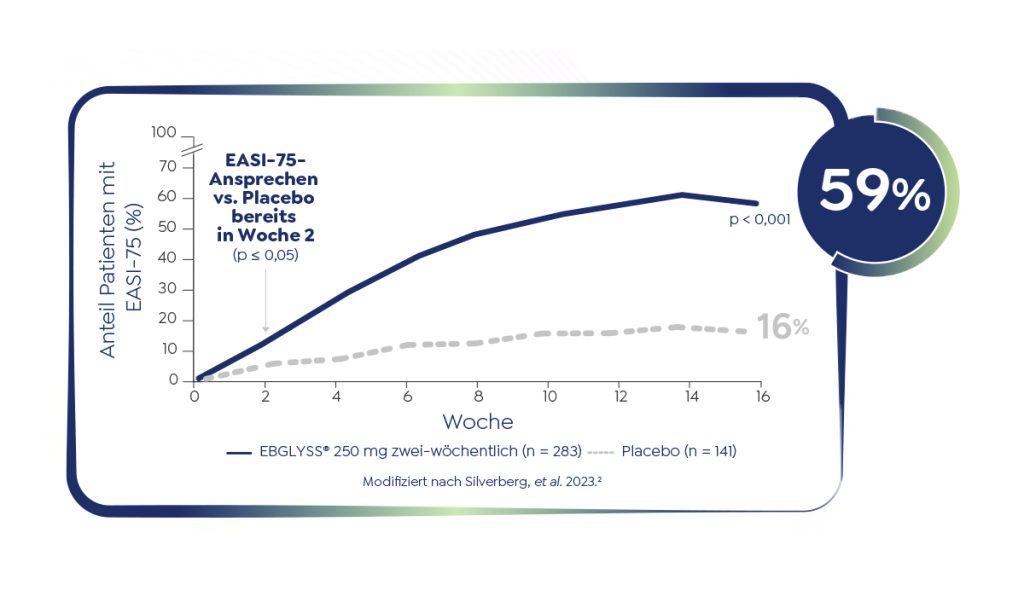
Starkes und frühes klinisches Ansprechen in der EBGLYSS®-Monotherapie
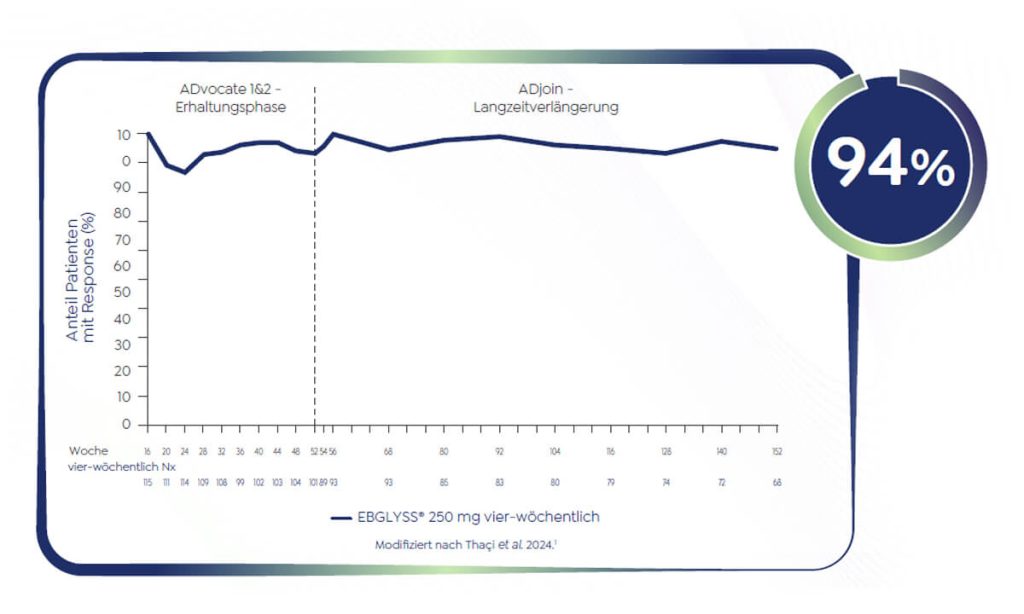
Langanhaltende Krankheitskontrolle über drei Jahre
Spürbare Linderung bei unerträglichem Pruritus
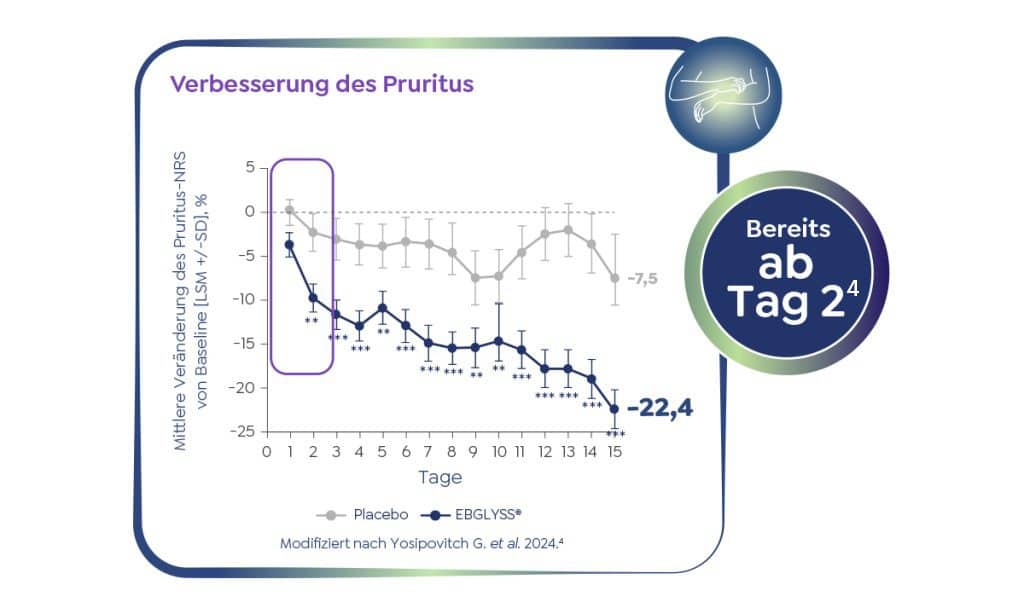
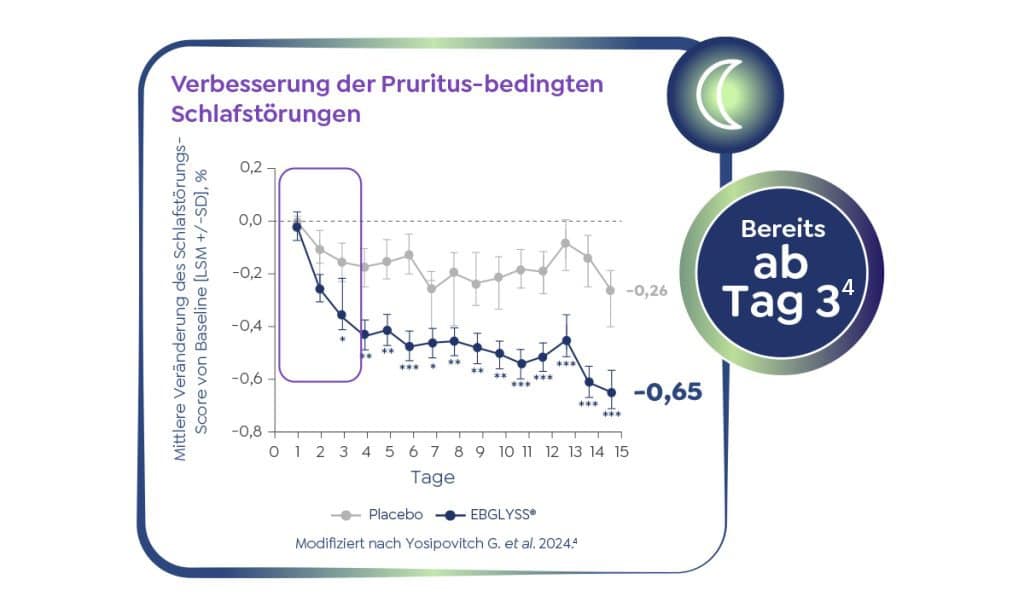
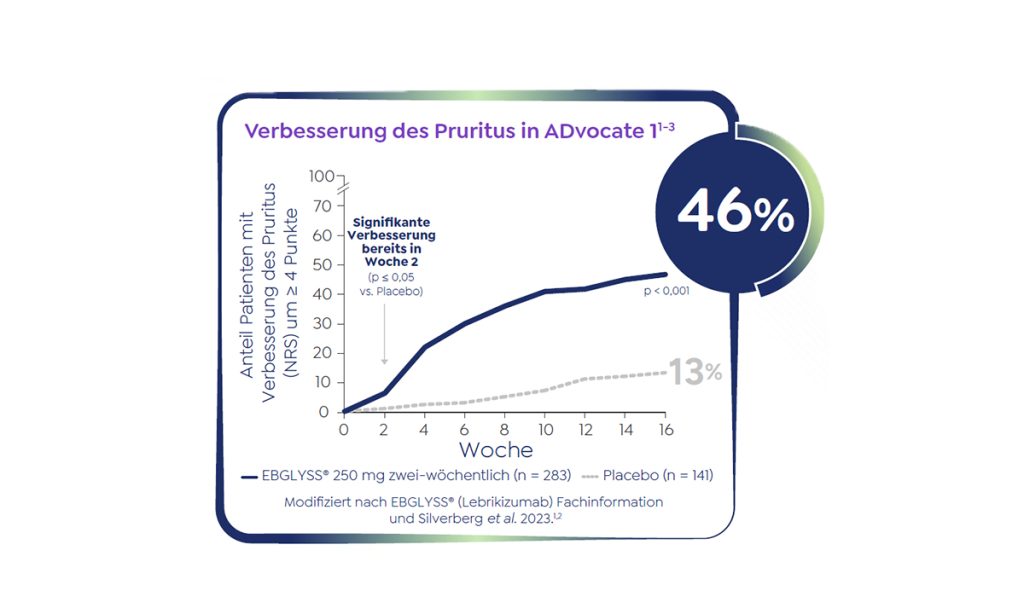
Spürbare Linderung des Pruritus bereits nach zwei Wochen mit EBGLYSS®
Fast die Hälfte der EBGLYSS®-Patient:innen erlebte in Woche 16 eine deutliche Verbesserung des Juckreizes in ADvocate 1.1-3
Starke Wirksamkeit im schwer zu behandelnden Gesichts- und Halsbereich8,9
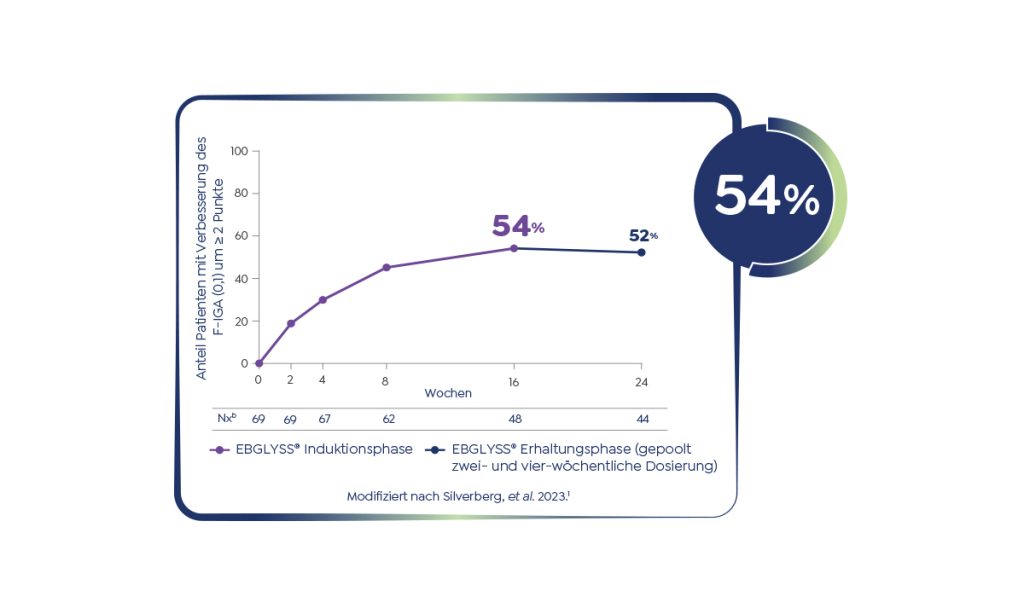
EBGLYSS® bietet eine bedeutende Verbesserung von atopischer Dermatitis im Gesicht - selbst bei Biologika-vorbehandelten Patienten10
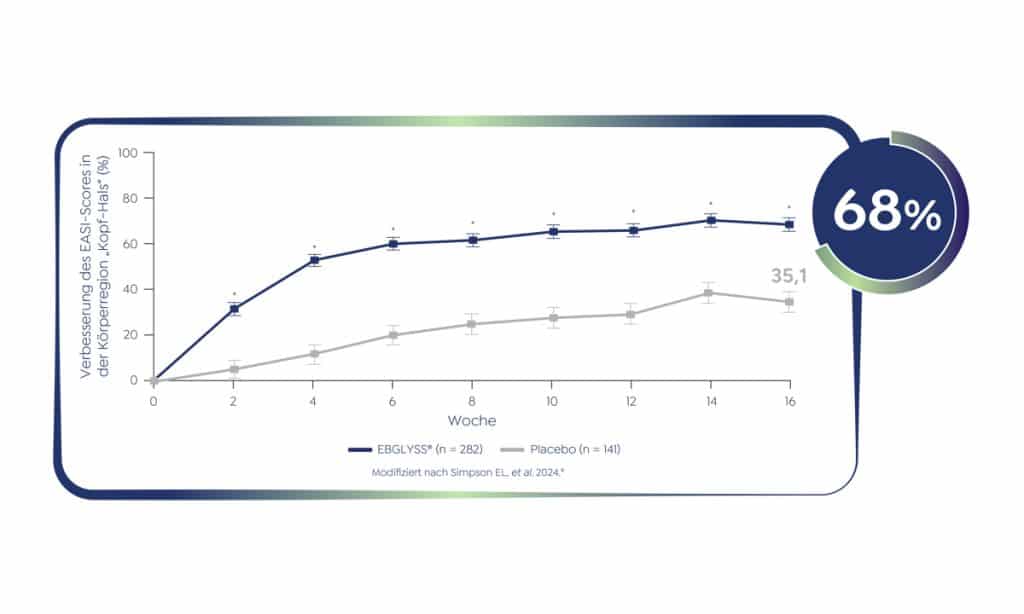
Starkes und frühes Ansprechen unter der EBGLYSS®- Monotherapie – auch im Gesichts- und Halsbereich
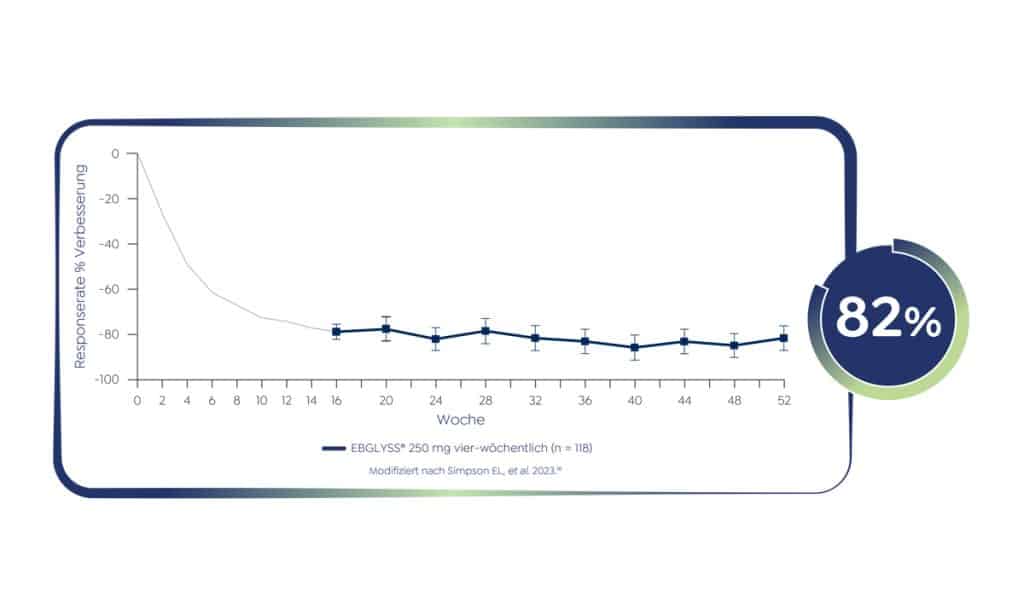
Langanhaltendes Ansprechen im Gesichts- und Halsbereich über 52 Wochen
EBGLYSS® weist ein überzeugendes Sicherheitsprofil auf.
Zugelassen ab zwölf Jahren1
Einfache Dosierung mit EBGLYSS®
EBGLYSS®: Dosierschema mit monatlicher Erhaltungstherapie für eine langanhaltende Krankheitskontrolle1
Die empfohlene Dosis von Lebrikizumab beträgt 500 mg (zwei 250 mg-Injektionen) in Woche null und Woche zwei, gefolgt von 250 mg subkutan alle zwei Wochen bis Woche 16.
Nach Erreichen der klinischen Response beträgt die empfohlene Erhaltungsdosis von EBGLYSS® 250 mg alle vier Wochen.

- EBGLYSS (Lebrikizumab). Fachinformation.
- Silverberg JI, et al. N Engl J Med. 2023 Mar 23;388(12):1080–1091.
- Silverberg JI, et al. N Engl J Med. 2023 Mar 23;388(12):1080–1091. Supplementary appendix.
- Yosipovitch G, et al. Br J Dermatol. 2024 Jan 23; 190(2): 289-291.
- BlauveltA, et al. Br J Dermatol. 2023 May 24;188(6):740–748.
- Thaçi D, et al. Efficacy and Safety of Lebrikizumab Is Maintained Up to 3 Years in Patients With Moderate-to-Severe Atopic Dermatitis: ADvocate 1 and ADvocate 2 to ADjoin Long-Term Extension Trial. Presented at the European Academy of Dermatology and Venereology (EADV); Amsterdam, Netherlands; September 25–28, 2024. D1T01.2.
- Murase JE, et al. Lebrikizumab-Treated Patients With Atopic Dermatitis Had No Increase in Treatment-Emergent Adverse Events of Facial, Head, and Neck Erythema Compared to Placebo. Presented at the Fall Clinical Dermatology Conference (Fall CDC 2023); Las Vegas, USA; 19 – 22 October 2023.
- Simpson EL, et al. Dermatol Ther (Heidelb). 2024 May; 14(5): 1145-1160.
- Simpson E, et al. Lebrikizumab reduces the extent of atopic dermatitis signs across body regions at 52/56 weeks. Presented at the 32nd European Academy of Dermatology and Venereology (EADV) Congress; Berlin, Germany; October 11 – 14, 2023. P0561.
- Silverberg J, et al. Presented at Fall Clinical 2024; Las Vegas, USA; 24–27 October 2024.
- Guttman-Yassky E et al. Poster presented at Fall CDC 2023; Las Vegas, USA; 19-22 October 2023.