In der vorliegenden Publikation beschreiben Hebert et al. die Ergebnisse einer Analyse der 16-Wochen-Daten der Phase-3-Studien ADvocate 1 & 2 sowie ADhere zur Wirksamkeit von Lebrikizumab speziell bei Heranwachsenden mit mittelschwerer bis schwerer atopischer Dermatitis (AD).
Die im November 2023 erteilte EU-Zulassung des monoklonalen Anti-Interleukin (IL)-13-Antikörpers Lebrikizumab zur Behandlung von erwachsenen und jugendlichen Patienten ab 12 Jahre mit einem Körpergewicht von mindestens 40 kg mit mittelschwerer bis schwerer AD stützte sich auf drei globale Phase-3-Studien: die Monotherapiestudien ADvocate 1 & 2 sowie die Studie ADhere zur Kombination mit topischen Kortikosteroiden (TCS). Die 16-Wochen- Daten der Heranwachsenden wurden von Hebert et al. separat analysiert und erstmals publiziert.
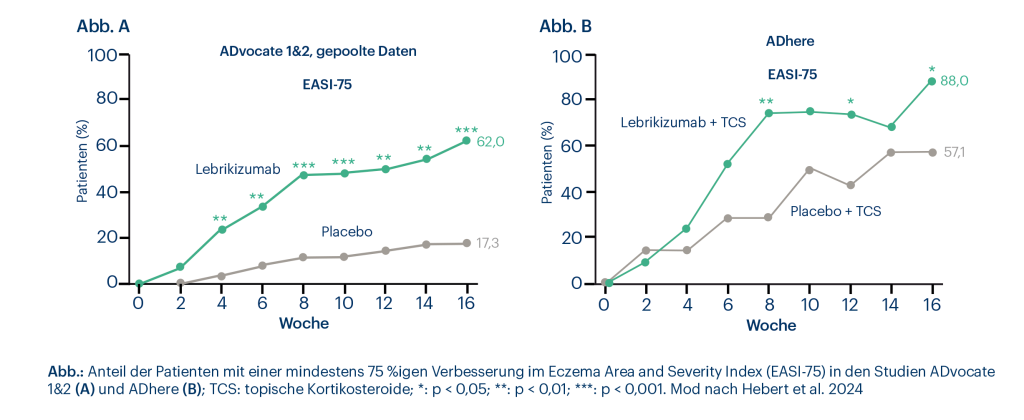
Die gepoolten Gruppen der beiden ADvocate-Studien umfassen 67 Heranwachsende in den Verum- und 35 in den Placeboarmen. In der ADhere-Studie hatten 32 Jugendliche Lebrikizumab 250 mg alle zwei Wochen s.c. (nach 500 mg in Woche 0 und 2) + TCS und 14 Jugendliche Placebo + TCS erhalten. In den ADvocate-Studien trat unter Lebrikizumab bis Woche 16 mit 62,0 % signifikant häufiger eine mindestens 75 %ige Verbesserung im Eczema Area and Severity Index (EASI-75) ein als unter Placebo mit 17,3 % (p<0,001) (Abb. A). Der Unterschied war bereits in Woche 4 signifikant (p<0,01). 40,7 % der Heranwachsenden zeigten unter Lebrikizumab in Woche 16 eine EASI-90-Response (Placebo: 11,5 %; p<0,01). In ADhere belief sich der Unterschied im EASI-75-Ansprechen in Woche 16 auf 88,0 % vs. 57,1 % (p<0,05) (Abb. B).
Mit einem Investigator’s Global Assessment (IGA)-Score von 0/1 (bei einer Verbesserung um mindestens zwei Punkte gegenüber Baseline) zeigte in ADvocate 1 & 2 in Woche 16 mit 46,6 % fast jeder zweite Patient eine nahezu oder vollständig erscheinungsfreie Haut (Placebo: 14,3 %, p < 0,01). In ADhere betrug dieser Anteil 57,3 % vs. 28,6 %; (p = 0,104).
Hinsichtlich der von den Patienten berichteten Therapieeffekte ging der Pruritus auf einer von 0 – 10 reichenden Numerischen Bewertungsskala (NRS) in ADvocate 1&2 unter Lebrikizumab bis Woche 16 bei 48,9 % der Heranwachsenden um ≥ 4 Stufen zurück (Placebo: 13,1 %; p < 0,01). In ADhere belief sich der Unterschied auf 45,8 % vs. 13,8 % (p = 0,088). In einem Score zum Schlafverlust verbesserten sich Patienten unter Lebrikizumab ebenfalls häufiger als unter Placebo. Daten zur Verträglichkeit und Sicherheit werden in der Publikation nicht genannt.
Die Monotherapie mit Lebrikizumab bewirkt bei Heranwachsenden in Woche 16 signifikante Verbesserungen der Hautsymptome und des Juckreizes, lautet das Fazit der Autoren – mit signifikanten Effekten schon in Woche 4. In Kombination mit TCS waren die EASI-75 Ansprechraten höher als unter TCS allein. Die Ergebnisse stimmen mit den Daten zur Gesamtpopulationen der Studien überein. Lebrikizumab zeigt somit bei Heranwachsenden mit mittelschwerer bis schwerer AD als Monotherapie und auch in Kombination mit TCS eine robuste Wirksamkeit.
Quelle: Hebert, A.A., et al. (2024). “Efficacy of lebrikizumab in adolescent patients with moderate- to-severe atopic dermatitis: 16-week results from three randomized phase 3 clinical trials.” J Dermatol Treat 35: 2324833