Schuppenflechte – eine Volkskrankheit in der Hausarztpraxis
Autor und Bilderquelle: Dr. med. Viktor A. Czaika

Dr. med. Viktor A. Czaika
Facharzt für Dermatologie und Venerologie
Berlin
Vor dem Hintergrund einer Prävalenz von 1,5–4% in der europäischen Bevölkerung kann die Psoriasis vulgaris zu den wichtigen Volkskrankheiten unserer Zeit gezählt werden. Diese chronisch-entzündliche Systemerkrankung mit überwiegender Beteiligung der Haut und der Gelenke ist sehr oft mit internistischen und neurologisch-psychiatrischen Komorbiditäten assoziiert und kann sogar Lebenszeitreduktion bedeuten.
Die manifeste Psoriasis beeinflusst alle Bereiche der Lebensqualität der Betroffenen mit negativer Auswirkung auf das physische, psychische, soziale und sexuelle Wohlbefinden. Die Vielzahl der Patienten steht einer sehr eingeschränkten dermatologisch-fachärztlichen Versorgungskapazität gegenüber. Daher ist interdisziplinäre ärztliche Zusammenarbeit wichtig. Im Folgenden sollen Handlungsempfehlungen für die Erstdiagnostik, weitere Diagnostik und Therapieeinleitung bei Schuppenflechte in der Hausarztpraxis dargelegt werden, wobei das besondere Augenmerk auf dem Potenzial der Lokaltherapie liegt.
Psoriasis und das Erfordernis einer interdisziplinär-kollegialen Versorgung
Ein Grundproblem wird in der Hausarztpraxis immer deutlicher: Das Problem zeitnaher und bedarfsgerechter Facharzttermine. Immer wieder wird dies besonders bezüglich der Hautfacharztvorstellung beklagt. Die an Hauterkrankungen und Allergien leidenden Patientinnen und Patienten wenden sich in aller Regel hilfesuchend an ihre Hausärztin bzw. ihren Hausarzt, die zunehmend und zwangsläufig dermatologische Aufgaben übernehmen müssen. Dies gilt in besonderem Maße auch für das Krankheitsbild der Psoriasis vulgaris. Von den etwa zwei Millionen Betroffenen in Deutschland befindet sich etwa ein Drittel nicht in dermatologischer Behandlung.
Die große Anzahl der Betroffenen, immerhin 2,5% der Bevölkerung in Deutschland, und der hohe Leidensdruck der Patientinnen und Patienten machen es verständlich, dass inzwischen von einer Volkskrankheit gesprochen wird. Die Psoriasis ist die erste Hauterkrankung, die von der WHO als „nicht übertragbare Krankheit (NCD)“ anerkannt ist, die – wie auch Diabetes mellitus, kardiovaskuläre Erkrankungen, Krebs und Erkrankungen der Atemwege – größerer Aufmerksamkeit bedarf. Der Krankheitswert der Psoriasis geht weit über die kosmetische und damit erhebliche psychische Belastung für die Betroffenen hinaus. Denn als chronisch-entzündliche Systemerkrankung leistet sie unbehandelt einer Vielzahl von kardiovaskulären, muskuloskelettalen, gastrointestinalen, psychiatrischen und anderen Komorbiditäten Vorschub. Zusammenhänge einer langfristig unbehandelten Psoriasis mit einem signifikant erhöhten Myokardinfarktrisiko, chronisch entzündlichen Darmerkrankungen, Diabetes mellitus, Depression u. a. sind wissenschaftlich bewiesen. Eine langfristig unbehandelte aktive Psoriasis kann eine Verkürzung der Lebenserwartung bedeuten [15]. Dies erklärt, warum die Psoriasis längst ein interdisziplinäres medizinisches Problem darstellt, das auch der interdisziplinären ärztlichen Behandlung und Betreuung bedarf. In diesem Kontext nimmt die Hausarztmedizin zunehmend eine Schlüsselposition ein. Der folgende Beitrag soll gleichzeitig praxisorientierte Übersicht und Handlungsleitfaden für die frühe Erkennung, die richtige Stadienzuordnung und die initiale Therapieeinleitung bei Psoriasis vulgaris darstellen. Eine besondere Bedeutung erlangt in diesem Zusammenhang die antipsoriatische Lokaltherapie.
Definition und Einteilung der Psoriasis
Die Psoriasis ist eine entzündliche chronisch-rezidivierende, immunologische Systemerkrankung, die vor allem die Haut, aber auch Nägel (30 %) und Gelenke (20%) betrifft [1]. Sie ist genetisch determiniert und wird durch endogene und exogene Triggerfaktoren ausgelöst oder unterhalten. Die typische Leiteffloreszenz sind elevierte erythematöse Plaques mit silberweiß- glänzender Schuppung, die symmetrische Streckseitenbetonung ist die typische Manifestationscharakteristik.
Bei einer geschlechtsunabhängigen Prävalenz von 2–3% in Deutschland gibt es zwei Altersgipfel des Erstauftretens. Die Typ-1-Psoriasis (60–70% der Fälle) manifestiert sich um das 10.–25. Lebensjahr, während die Typ-2-Psoriasis sich um das 40.–60. Lebensjahr manifestiert. Die Mehrzahl der Betroffenen wird ab dem 40. Lebensjahr symptomatisch. Die frühe Form zeigt familiäre Häufung, geht mit HLA-Assoziation (Cw6, B13, B57, DrB1) einher und verläuft zumeist schwerer mit häufigerer Gelenkbeteiligung. Die späte Form nimmt zumeist leichtere Verläufe, und die Gelenke sind seltener betroffen.
Die Psoriasis vulgaris wird in die Schweregrade „leicht“, „mittelschwer“ und „schwer“ unterteilt. Diese Einteilung ist vor allem relevant für die Therapieentscheidung [3, 16].
Nach europäischem Konsensus wird die Zuordnung durch drei Scores definiert: der Body Surface Index (BSA) erfasst die betroffene Körperoberfläche (0–100%). Der PASI-Index (Psoriasis Area and Severity Index) wird aus der Rötung der Haut, der Dicke der Plaques, dem Ausmaß der Schuppung sowie dem Anteil der betroffenen Körperoberfläche berechnet. In Analogie wurde speziell für die Kopfhautpsoriasis der PSSI (Psoriasis Scalp Severity Index) entwickelt. Ist der PASI höher als zehn Punkte, liegt eine mittelschwere bis schwere Schuppenflechte vor. Der Dermatology Life Quality Index (DLQI) spiegelt die Stärke der Einschränkung der Lebensqualität durch die Schuppenflechte wider, die von BSA und PASI nicht berücksichtigt wird. Der Patientenfragebogen zu den vergangenen sieben Tagen thematisiert unter anderem den Beruf, die Partnerschaft, die Freizeit und die Behandlung (Tab. 1).
Tabelle 1: Schweregradeinteilung der Psoriasis vulgaris entsprechend den verschiedenen Scores. Bei leichter Psoriasis müssen alle Scores einen Wert „≤ 10“ ergeben.
Für die klinische Einteilung ist die Unterscheidung der Psoriasis vulgaris (Pso) von der Psoriasis arthropathica (PsoA) grundlegend entscheidend. Die Hautmanifestation bei Schuppenflechte kann therapeutisch immer wieder bis zur Erscheinungsfreiheit zurückgedrängt werden, einmal entstandene morphologische Gelenkveränderungen hingegen sind irreversibel.
Die Psoriasis ist eine T-Zell-vermittelte Autoimmunerkrankung, bei der T-Lymphozyten und antigenpräsentierende Zellen aktiviert werden. Das konkrete Antigen konnte bislang nicht identifiziert werden. Die für die Beeinflussung der Funktion der Keratinozyten und Gefäßendothelien verantwortlichen Mediatoren jedoch sind bekannt und sind Angriffspunkt für eine Vielzahl hochwirksamer Antipsoriatika. Für die Polarisierung der T-Zellen in Richtung der für die Entstehung der Psoriasis relevanten Th1- und Th17-Zellen sind vor allem IFN-gamma, TNF-alpha, IL-12, IL-17, IL-22 und IL-23 verantwortlich. Dieser sich selbst potenzierende „Zytokincocktail“ verursacht die klinischen Auswirkungen: Die Entzündungsreaktion ist für die Entstehung der erythematösen Plaques und für den mehr oder weniger ausgeprägten Pruritus, aber auch für Enthesiopathie und Arthritis verantwortlich. Hyperproliferation und Differenzierungsstörung der Keratinozyten produzieren die charakteristische asbestweiße Schuppung. Die Ansammlung von neutrophilen Granulozyten lässt die histologisch sichtbaren Munro-Mikroabszesse, aber auch die bei Psoriasis-Sonderformen sichtbaren sterilen Pusteln entstehen (Psoriasis pustulosa).
Psoriasis vulgaris vom chronischen Plaque-Typ
Die Psoriasis vulgaris ist grundsätzlich eine klinische Diagnose, also eine Blickdiagnose. Nur in seltenen Fällen und bei Psoriasis-Sonderformen kann eine histologische Abklärung erforderlich werden.
Mit 90% aller Fälle ist die chronische Plaque-Psoriasis die häufigste Manifestationsform der Psoriasis vulgaris. Die hier geradezu pathognomonische Leiteffloreszenz ist die scharf begrenzte, erythematöse, 5–20 cm durchmessende Plaque mit charakteristischer groblamellärer, silberweißer Schuppung. Die Schuppung ist vor allem im Zentrum der Läsion ausgeprägt.
Praxistipp:
Mit wenigen Ausnahmen ist das Erkennen der Schuppenflechte eine klinische Blickdiagnose, die durch einfache unterstützende händische Tests untermauert werden kann. Es lassen sich die klassischen Kratzphänomene auslösen (Abb. 1).
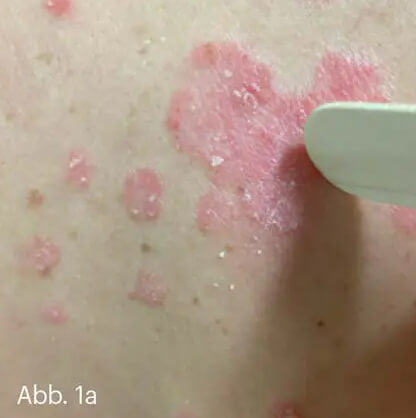
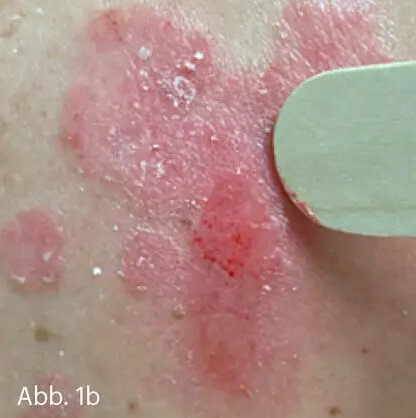
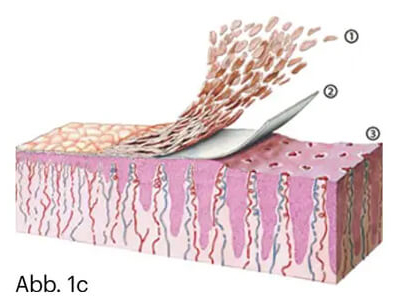
Ebenfalls charakteristisch ist die Verteilung der Plaques mit Manifestation an den Ellenbogen, den Knien, der Sakralregion und umbilikal sowie in den Gehörgängen und im Bereich der Kopfhaut mit Übergang auf den haarfreien Hautrand (Abb. 2).
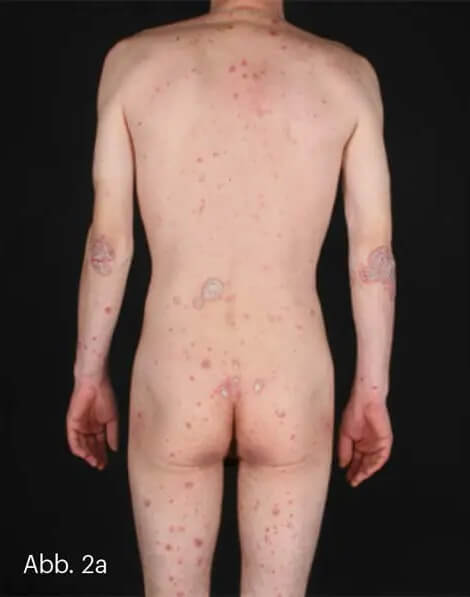
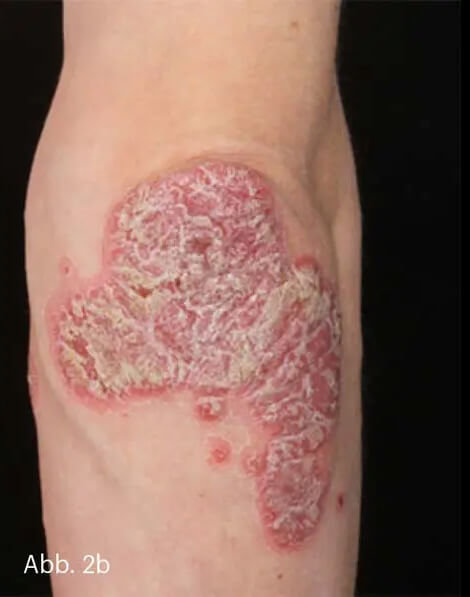
Abb. 2: 29-jähriger Patient mit chronischer Plaque-Psoriasis. Charakteristisch ist die Betonung der Extremitätenstreckseiten und der Sakralregion (a). Psoriasisplaque mit charakteristischer zentral betonter, mittel- bis groblamellärer Schuppung (b).
Bei großflächiger Ausdehnung mit Neigung zur Konfluenz entsteht ein landkartenartiger Eindruck, daher auch der Begriff „Psoriasis geografica“. Der Befall kann bis zum erythrodermatischen Aspekt heranreichen, ist aber von der Psoriasis erythrodermatica abzugrenzen (Abb. 3).
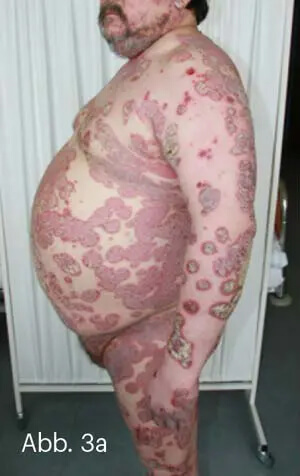
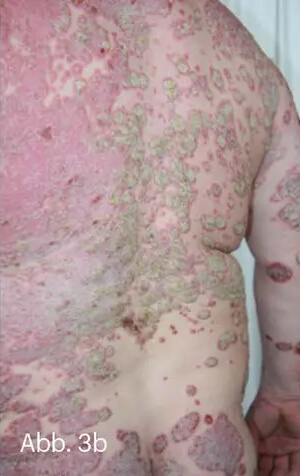
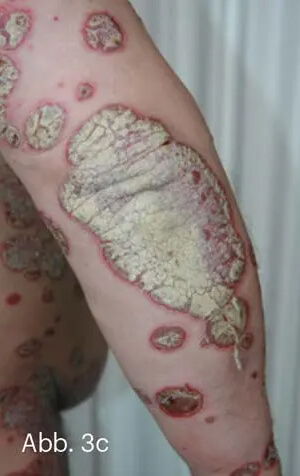
Abb. 3: Großflächig konfluierende Psoriasis vom chronischen Plaque-Typ (a, b). Die Konfluenz und der Aspekt der „Inseln vor der Küste“ ergeben den landkartenähnlichen Aspekt. Hier ausgeprägte groblamelläre, silberweiße Schuppung (c).
Das „Köbner-Phänomen“ ist der klinische Aspekt eines sogenannten isomorphen Reizeffektes. Dies ist die Neigung der Psoriasis, an unspezifisch, z. B. mechanisch, chemisch oder toxisch, irritierten Stellen zu entstehen, oft genau im Bereich der Einwirkung (Abb. 4).
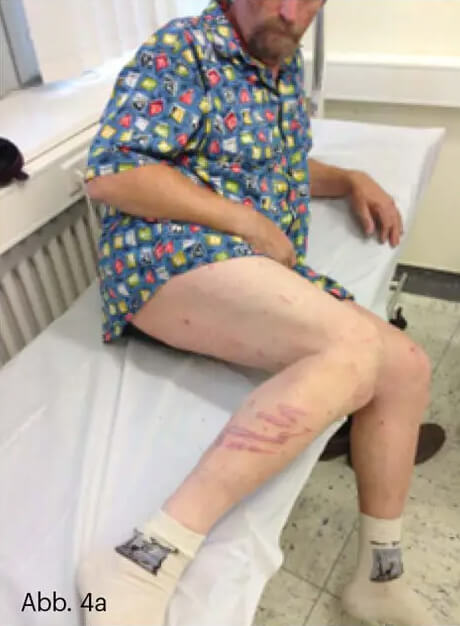
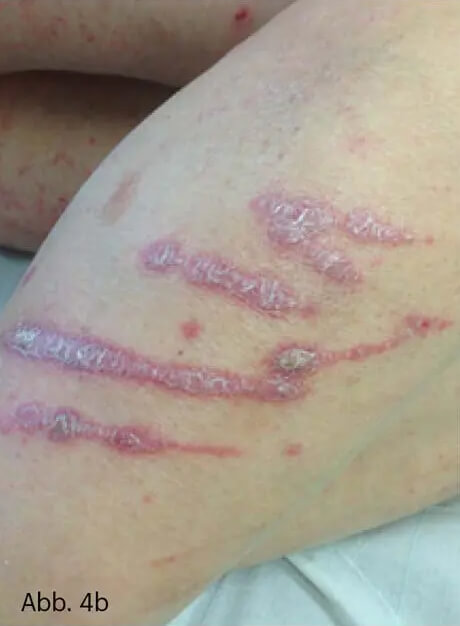

Abb. 4: Urlaubsrückkehrer von der nordafrikanischen Küste. Dort hatte er Kontakt zu einer „Portugiesischen Galeere“, einer Blasenquallenart. Zunächst hatten sich heftig entzündliche, streifige Rötungen aufgrund der Nesseltoxine der Quallententakel gebildet. Erst Tage später entwickelten sich genau in den Kontaktbereichen die bizarr konfigurierten psoriatischen Plaques (a–c).
Psoriasis inversa
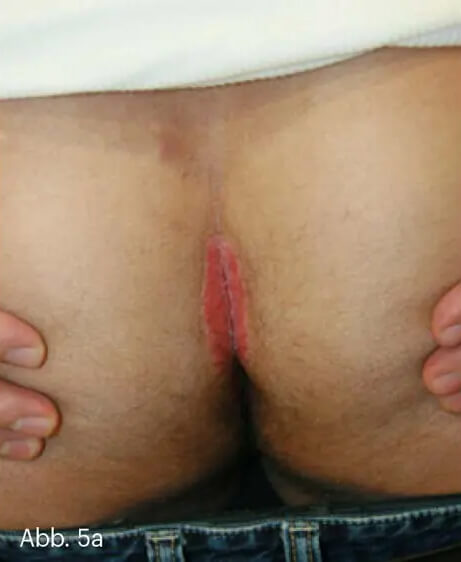
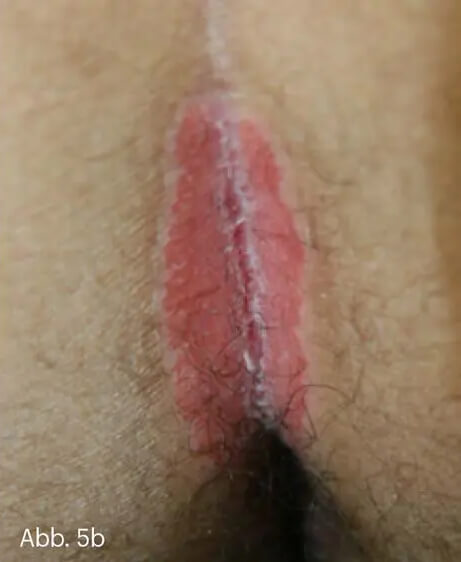
Abb. 5: Psoriasis inversa mit erythematöser Plaque. Hier zeigt sich eine randständig relativ gerade Begrenzung ohne Satellitenläsionen (a) und eine zentrale schmale Mazeration (b).
Seborrhiasis
Ein inverses Verteilungsmuster unter Beteiligung der seborrhoischen Areale des Gesichtes zeigt auch die sogenannte Seborrhiasis. Neben den Intertrigines sind oft auch großflächig die Prästernalregion und die dorsale Schweißrinne sowie die „T-Zone“ (nasolabial und Stirn) betroffen. Die Plaques sind flacher und haben einen düsterrot-entzündlich, ölig glänzenden Aspekt. Immer sollte hier eine HIV-Abklärung erfolgen, da Seborrhiasis eine typische Psoriasismanifestation bei HIV-Infektion ist. Eine plötzlich und massiv auftretende Psoriasis inversa und auch ein akut aufschießendes seborrhoisches Ekzem zählen nach CDC (Center of Disease Control) zu den frühen Indikatorkrankheiten für AIDS (Abb. 6).
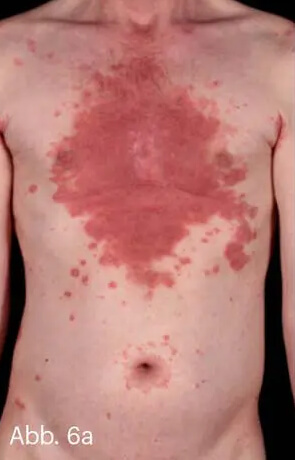
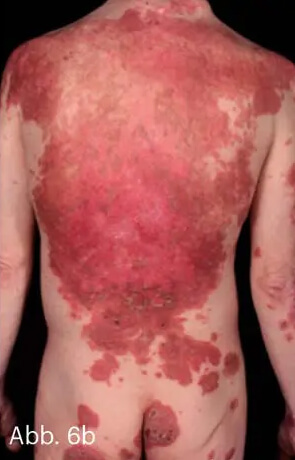
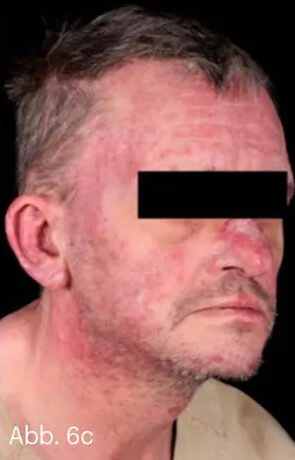
Abb. 6: „Seborrhiasis“ bei einem 34-jährigen Patienten mit HIV-Infektion. Charakteristisch ist der entzündliche, eher diskret schuppende Aspekt der Läsion in Projektion auf die seborrhoischen Areale (a–c).
Psoriasis palmoplantaris
Die Psoriasis palmoplantaris ist der Befall der Hand- und Fußflächen und kommt bei etwa 15% der Patientinnen und Patienten mit Psoriasis vor. Typisch ist der Beginn in der Mitte von Hand- oder Fußsohlen, die Plaques sind jeweils scharf begrenzt. Die massiv hyperkeratotischen, erythematösen Plaques können tiefe, schmerzhafte Rhagaden aufweisen. Diese Manifestationsform kann auch isoliert auftreten. Dann ist die klinische Differenzialdiagnose zum hyperkeratotischen Hand- und Fußekzem, aber auch zur „Mokassin-Mykose“ durch anthropophile Dermatophyten besonders schwierig (Abb. 7).
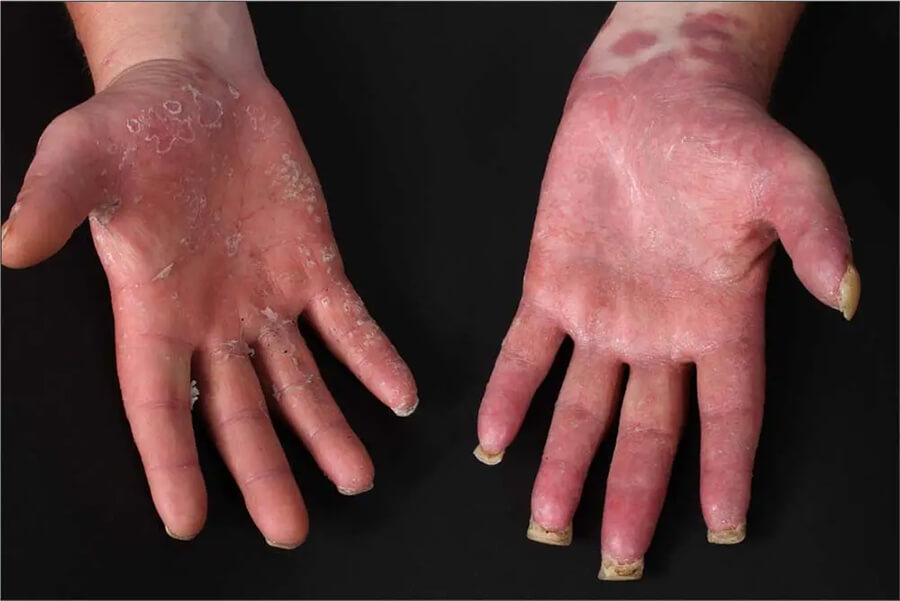
Abb. 7: Palmare Psoriasismanifestation. Die Unterscheidung zum irritativ-toxischen Handekzem ist hier schwierig.
Psoriasis pustulosa
Seltener ist der palmoplantare Befall durch das Auftreten steriler Pusteln charakterisiert. Hier handelt es sich um das Bild der Psoriasis pustulosa palmoplantaris. Die Pathophysiologie ist nicht zur Gänze geklärt, die Pusteln sind das Ergebnis des massiven Einstroms von Neutrophilen (Abb. 8). Insbesondere das dyshidrotische Hand- und Fußekzem ist hier eine wichtige Differenzialdiagnose.
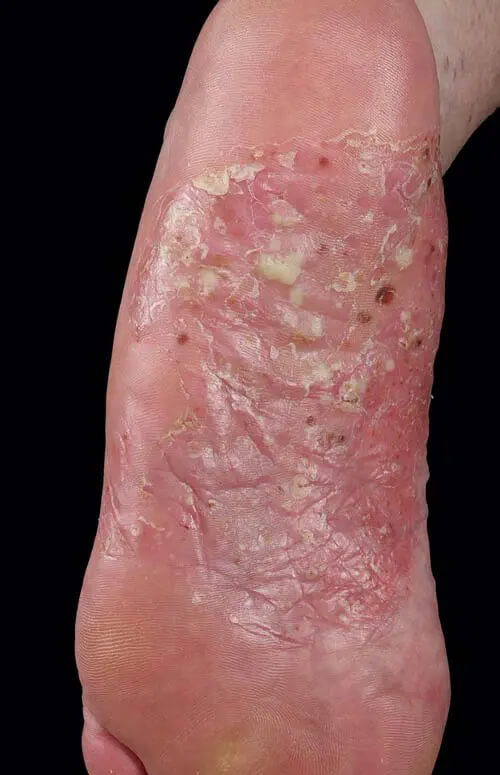
Abb. 8: Psoriasis pustulosa plantaris mit charakteristischer Ausprägung in der Fußsohlenmitte und nicht follikulär gebundenen (sterilen) Pusteln.
Die Psoriasis pustulosa palmoplantaris ist die lokalisierte Form der pustulösen Psoriasis, die der sehr seltenen Psoriasis pustulosa generalisata (GPP) gegenüberzustellen ist. Die GPP ist ein fieberhaftes, potenziell letales Krankheitsbild mit extremer Linksverschiebung im Entzündungslabor, Fieber, Arthritis und weiteren Systemzeichen. Insbesondere besteht zumeist ein schwer reduzierter Allgemeinzustand. Generalisiert treten großflächige Erytheme mit multiplen, disseminierten, nicht follikulär gebundenen Pusteln auf, die zu regelrechten „Pustel-Seen“ konfluieren können. Der Stamm und die Extremitäten sind bevorzugt befallen, aber auch die Schleimhäute und sogar die Atemwege können betroffen sein. Trigger sind Infekte, Medikamente, Stress und sogar eine Schwangerschaft. Zwar leiden einige der Betroffenen zuvor an einer Psoriasis vulgaris, dennoch wird die GPP als eigenständige Entität gesehen. Gute Erfolge gibt es derzeit mit dem Einsatz von Anti-IL-36-Antikörpern entsprechend dem hier permanent pathologisch aktivierten IL-36-Signalweg. Die AGEP (akute generalisierte exanthematische Pustulose) ist in diesem Zusammenhang speziell die Unverträglichkeitsreaktion auf Arzneimittel wie Lithium, Methotrexat, Penicillin u. a.
Psoriasis exanthematica
Die Psoriasis exanthematica ist eine akut aufschießende, zumeist durch Infekte getriggerte Psoriasis. Stammbetont manifestieren sich maximal 1–2 cm große, „tropfenförmige“, flache Plaques. Daher wird diese Form der Psoriasis auch Psoriasis guttata (lat. gutta = Tropfen) genannt. Typisch ist sie als Psoriasis-Erstmanifestation im Kindesalter nach Streptokokkeninfekten, sie kann aber auch bei Erwachsenen auftreten (Abb. 9).
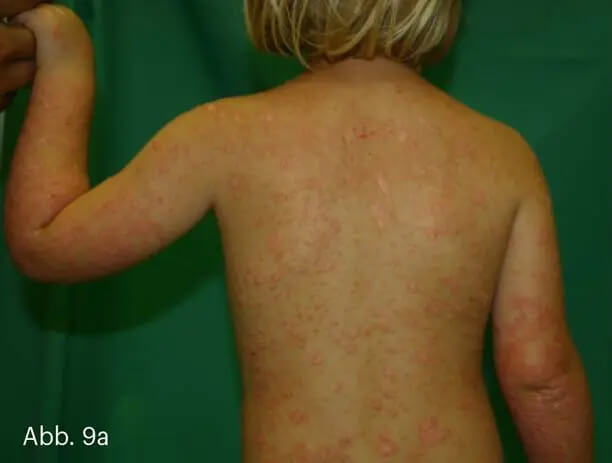
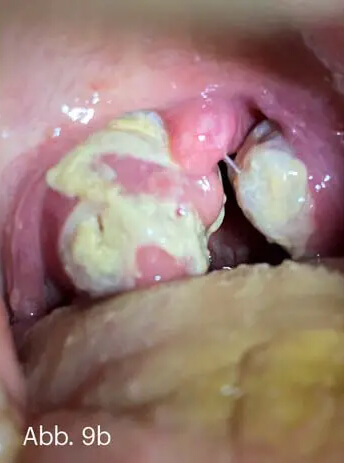
Abb. 9 Psoriasis exanthematica bei einem Kleinkind. Typisch ist die dissimilierte Aussaat der schuppenden ovalären Plaques (a). Auslöser war eine streptogene Angina tonsillaris (b).
Die Psoriasis guttata kann leicht mit der Pityriasis rosea verwechselt werden, einer HHV-6-Infektion bei jüngeren Menschen mit ebenfalls stammbetonten schuppenden Plaques. Hier kann allerdings oft ein vorangehender primärer Herd („Primärmedaillon“) eruiert werden, und die ebenfalls exanthematisch auftretenden Läsionen haben einen typischen Verlauf entlang der Hautspaltlinien. Gerade bei Kleinkindern ist immer auch an eine Mikrosporie („Katzenpilz“) zu denken, eine sich rasch ausbreitende und durch Katzen und Hunde übertragene zoophile Dermatophytose durch Microsporum canis. Allerdings sind oft nicht vorrangig bzw. primär die Extremitäten betroffen, sondern eher Rumpf und Gesicht sowie der behaarte Kopf, Symmetrie fehlt. Aber auch die atopische Dermatitis und die Pityriasis lichenoides varioliformis (eine den Windpocken ähnelnde entzündliche Dermatose unklarer Ätiologie) sind abzugrenzen.
Psoriasis erythrodermatica
Im Gegensatz zur großflächigen Psoriasis vom stationär-chronischen Typ ist die Psoriasis erythrodermatica durch ein hochentzündliches Erythem von mindestens 70% der Körperoberfläche charakterisiert und definiert. Durch die Entzündungsreaktion mit großflächiger Vasodilatation sind Wasser- und Proteinverlust und eine gestörte Wärmeregulation zu erklären. Die Betroffenen haben ein starkes Krankheitsgefühl und entwickeln Fieber und Schüttelfrost. Da das Krankheitsbild auf der primären Grundlage der Psoriasis entsteht, handelt es sich um eine sekundäre Erythrodermie (Abb. 10). Die Abgrenzung von anderen Erythrodermien ist schwierig.
Weitere sekundäre Erythrodermien können vor dem Hintergrund einer atopischen Dermatitis, eines seborrhoischen Ekzems, eines systemischen Lupus erythematodes (SLE), einer Dermatomyositis oder auch einer Skabies entstehen. Abzugrenzende primäre Erythrodermien wären die Psoriasis pustulosa generalisata, das Stevens-Johnson-Syndrom (SJS) und die toxische epidermale Nekrolyse (TEN), das Sézary-Syndrom (erythrodermische Variante der Mycosis fungoides), eine Ichthyosis u. a. Eine Erythrodermie ist unabhängig von ihrer Ursache bzw. Genese immer als klinischer Notfall einzustufen und muss stationär versorgt werden.
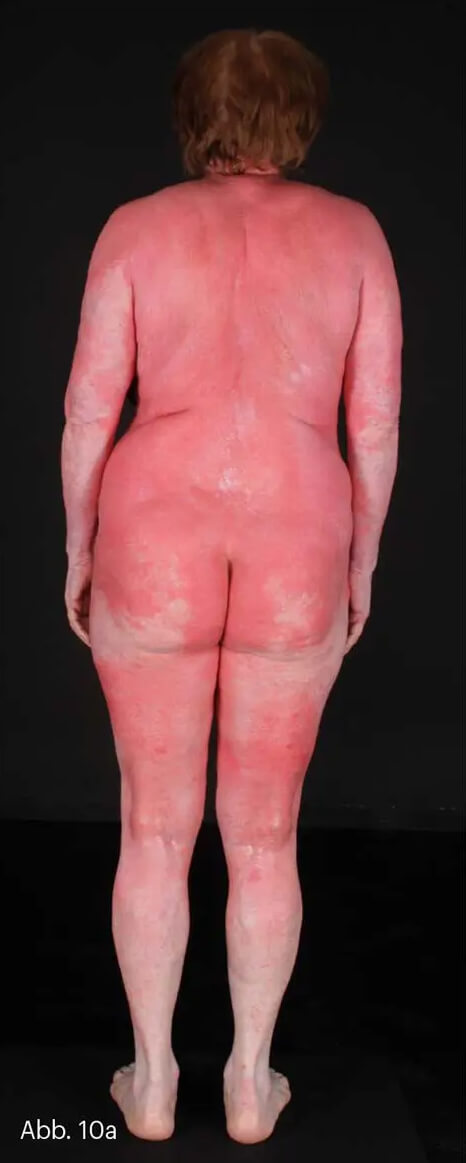
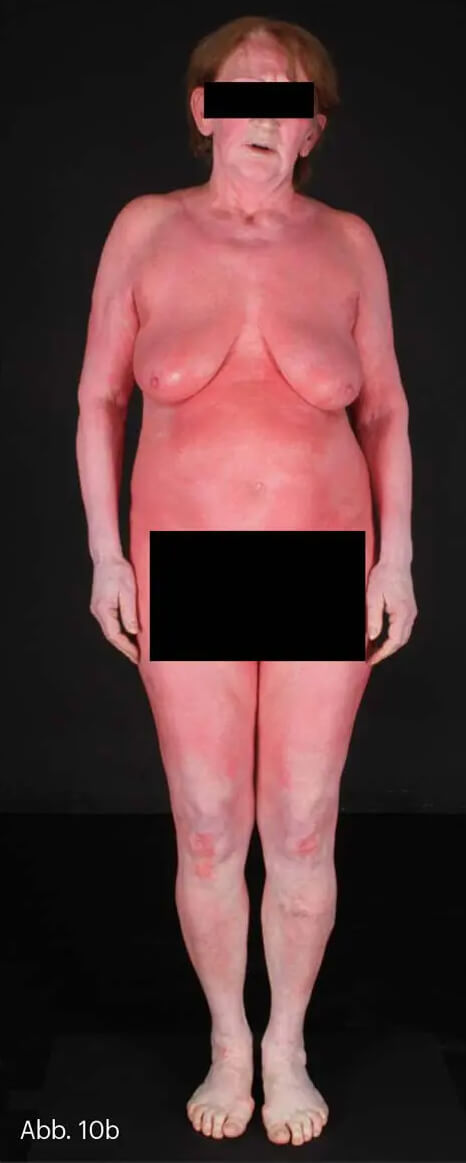
Abb. 10: Psoriasis erythrodermatica mit Befall des nahezu gesamten Integuments (a, b).
Nagelpsoriasis
Neben der Haut manifestiert sich die Psoriasis vulgaris häufig (etwa 50%) an den Nägeln. Die Korrelation psoriatischer Gelenk- und Nagelveränderungen liegt bei 80–90%.
Das Ausmaß der Veränderungen reicht von nur diskret bis hin zur ausgeprägten Onychodystrophie. Es können einzelne, aber auch alle Nägel verändert sein. Nagelbefall stellt eine besondere psychische Belastung für die Betroffenen dar, da auch hier im Laienverständnis von mangelnder Pflege oder einer ansteckenden Pilzinfektion ausgegangen und der direkte Kontakt gemieden wird. Nägel mit punktuellen Grübchen der Nagelplatte werden auch „Tüpfelnägel“ genannt und stellen eine psoriatische Störung der Nagelmatrix dar. Progredienz führt zu Riffelung und kompletter Onychodystrophie („Krümelnägel“) (Abb. 11).
Praxistipp:
Daher gilt der Grundsatz: „Die Nägel sehen, an die Gelenke denken!“
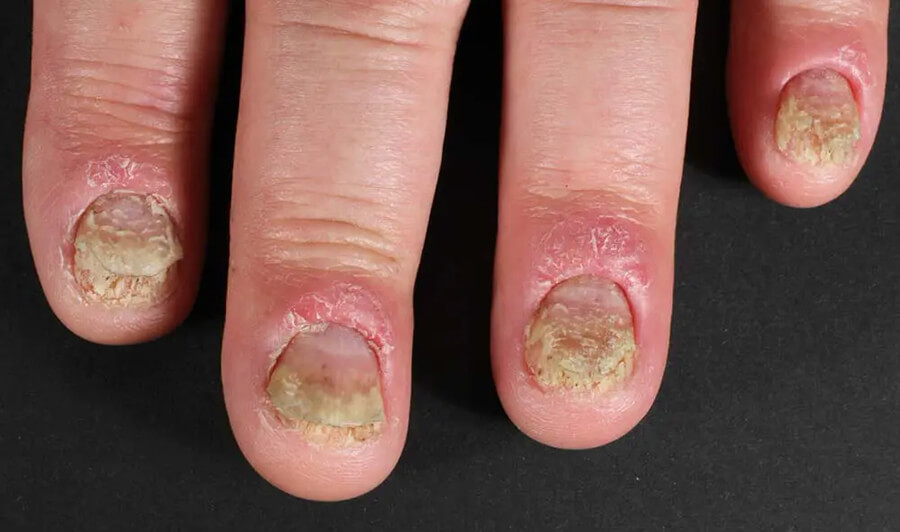
Abb. 11: Nagelpsoriasis mit erheblicher Onychodyschromasie und Onychodystrophie. Dig. II mit angedeutetem Ölflecken-Phänomen, Dig. V mit psoriatischer „Tüpfelung“.
Störungen der Nagelmatrix hingegen verursachen das sogenannte „Ölflecken-Phänomen“, bräunliche, subunguale Flecken und großflächige, weißliche Onycholysen, die durch die subungualen Hyperkeratosen verursacht werden. Die Differenzialdiagnosen sind in Tabelle 2 dargestellt.
Tabelle 2: Differenzialdiagnosen wichtiger Nagelerkrankungen.
Praxistipp:
Typischerweise beginnen die Nagelveränderungen bei Psoriasis an den Händen und später erst an den Füßen, da die Fingernägel schneller wachsen. Bei der Onychomykose ist die zeitliche Reihung genau andersherum, d. h., üblicherweise sind erst die Fußnägel und dann die Fingernägel betroffen.
Psoriasis arthropathica
Etwa ein Fünftel aller von Psoriasis Betroffenen entwickelt eine Arthritis psoriatica [1]. Gelenkbeschwerden, psoriatische Plaques an den Händen und Füßen (vor allem perionychial) sowie Nagelveränderungen sollten immer Anlass sein, eine mögliche Psoriasisarthritis abzuklären. Dabei schließt ein unauffälliges Röntgenbild diese keineswegs aus. Wichtig ist es, die frühen Weichteilbeschwerden zu erfragen. Morgensteifigkeit der Fingergelenke, Schwellungen der Finger oder Zehen (Daktylitis) und Enthesitis (Sehnenansatzschmerzen) sind Warnzeichen (Abb. 12). Die Arthritis psoriatica ist seronegativ, d. h., im Rheumalabor finden sich (ggf. mit Ausnahme von HLA-B27 bei Sakroiliitis) negative Befunde. Dabei ist insbesondere die Abgrenzung von der rheumatoiden Arthritis (RA) nicht leicht.
Praxistipp:
Daktylitis mit homogener Schwellung des gesamten Fingers bzw. der Zehe sprechen für Psoriasisarthritis („Wurstfinger“). Schwellungen nur über den proximalen Interphalangealgelenken (PIP) sprechen eher für RA.
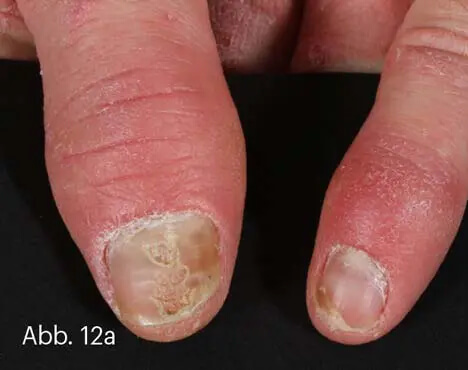
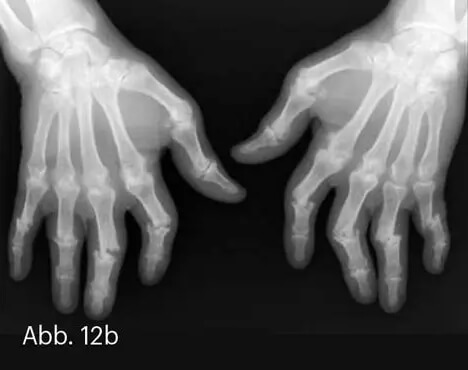
Abb. 12: Arthritis psoriatica vom polyarthritischen Typ mit spindelförmiger entzündlicher Schwellung („Wurstfinger“) (a). Ausgeprägte ossäre Mutilationen einer unbehandelten Psoriasis arthropathica bei einem anderen Patienten (b).
Bei der Gelenkpsoriasis werden verschiedenen Formen unterschieden (Tabelle 3).
Tabelle 3: Klinische Varianten der Arthritis psoriatica. DIP-Gelenke: distale Interphalangealgelenke.
Da es keine bindenden Diagnosekriterien gibt, handelt es sich um eine Ausschlussdiagnose. Entsprechend den CASPAR-Kriterien gilt folgende Regel: Eine Psoriasis arthropathica ist wahrscheinlich bei bestehender entzündlich-muskuloskelettaler Erkrankung und Nachweis von drei der folgenden Erkrankungen: Psoriasis der Haut (auch Anamnese), Nagelpsoriasis, negativer Rheumafaktor (RF), Daktylitis, Röntgenbild mit juxtaartikulärem Knochenumbau. Für eine genauere Analyse und bei Studienfragen sind verschiedene validierte Fragebögen verfügbar, z. B. der deutschsprachige PsA-Screening-Fragebogen GEPARD oder der PEST-Fragebogen (psoriasis epidemiology screening tool) [17, 18].
Es gilt auch zu bedenken, dass rein kutane psoriatische Hautmanifestationen dem Gelenkbefall um 5–10 Jahre vorausgehen können. Die Typ-1-Psoriasis jüngerer Patienten hat eine höhere Wahrscheinlichkeit für eine Gelenkmanifestation.
Praxistipp:
Gelenkschmerzen bei Psoriasis sollten immer als Arthritis psoriatica gewertet werden, solange nicht andere schlüssige Ursachen gefunden werden.
Komorbiditäten oder „Psoriasis als Spitze des Eisbergs“
Die Psoriasis wurde bereits vom griechischen Arzt Hippokrates (ca. 460–370 v. Chr.) beschrieben und ist damit seit weit über 2.000 Jahren bekannt. Ebenso lange allerdings galt sie auch als reine Hauterkrankung und eher als hauptsächlich kosmetisch-ästhetisches Problem. Erst in den letzten Jahren hat sich das Verständnis der „Schuppenflechte“ von Grund auf gewandelt. Eine Vielzahl von proinflammatorischen Molekülen, hauptsächlich TNF-alpha, IL-6 oder IL-17 und IL-23, vermitteln die Entzündungen in der Haut mit Entwicklung der psoriatischen Plaques. Die gleichen Moleküle und Mediatoren aber sind auch verantwortlich für die Entstehung und Progredienz internistischer Krankheitsbilder. Diese internistischen Abläufe verstärken sich unter dem Entzündungsdruck bei ausgeprägter Psoriasis. Mit anderen Worten, je ausgeprägter die Psoriasis, desto wahrscheinlicher das Voranschreiten der Komorbiditäten. Zu den wichtigen Komorbiditäten zählen zum einen die Bestandteile des metabolischen Syndroms, die bei Psoriatikern nicht selten vollzählig vertreten sind: arterielle Hypertension, Dyslipidämie, Diabetes mellitus und Adipositas (Abb. 13). Insbesondere Psoriasis und Adipositas leisten der Insulinresistenz mit konsekutiven Endothelschäden, Atherosklerose und hohem Risiko für Myokardinfarkt und Schlaganfall Vorschub. Diese Kaskade verbirgt sich hinter der Begrifflichkeit des „psoriatischen Marsches“ [19]. Inzwischen wird eine Neigung zur Tumorentstehung mit unbehandelter Psoriasis assoziiert. Zu den Komorbiditäten zählen aber auch die Neigung zu chronisch-entzündlichen Systemerkrankungen wie Colitis ulcerosa und Morbus Crohn [20] sowie eine erhöhte Inzidenz von Depressionen, die nicht ausschließlich als reaktiv zu erklären sind [21, 22]. Einige Autoren rechnen auch die Arthritis psoriatica zu den Komorbiditäten. In Studien konnte gezeigt werden, dass das Risiko für das Erleiden eines Myokardinfarkts schon bei jungen Psoriatikern ohne weitere Risikofaktoren bis um den Faktor drei erhöht ist. Es besteht ein doppelt so hohes Risiko, an Diabetes zu erkranken. Patienten mit schwerer Psoriasis sterben 4–7 Jahre früher im Vergleich zur Normalbevölkerung [4].
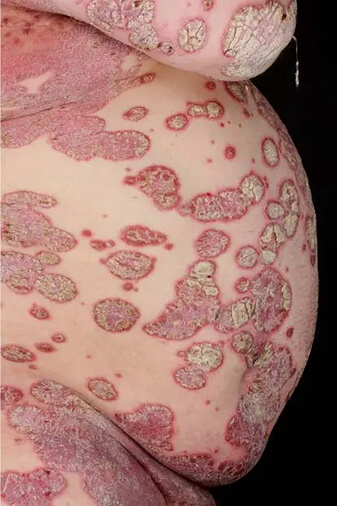
Abb. 13: 57-jähriger Patient mit Assoziation von „Psoriasis geographica“ mit ausgeprägtem metabolischen Syndrom. Der vergrößerte Bauchumfang („Apfeltyp“) ist charakteristischer Hinweis auf ausgeprägtes, metabolisch ungünstiges Viszeralfett.
Merke: „Psoriasis geht unter die Haut!“
Therapie der Psoriasis
Die mittelschwere bzw. schwere Schuppenflechte stellt unter Berücksichtigung eventueller Kontraindikationen eine mögliche bzw. absolute Indikation zur Systemtherapie dar. Ungeachtet dessen jedoch werden nur etwa 10% der an Psoriasis Erkrankten derzeit systemisch behandelt! In den letzten Jahren galt das Hauptaugenmerk der Leitlinien fast ausschließlich den Systemtherapeutika. Die Grundsätze zur Systemtherapie sind in der 2021 entstandenen Neuauflage der S3-Leitlinie zur Diagnostik und Therapie der Psoriasis dargelegt. Doch inzwischen erlebt die Beachtung der topischen Behandlung der Psoriasis eine Renaissance, da sie bei jeder Patientin und jedem Patienten mit Psoriasis grundsätzlich und nahezu unbedenklich angewendet werden kann. Sie stellt eine wesentliche Therapieoption auch in der hausärztlichen Praxis dar. Und es ist zu wünschen, dass die Lokaltherapie in der derzeitigen erneuten Überarbeitung der Psoriasisleitlinie eine klarere Darlegung erfährt [3, 4].
Biologika
Die Entwicklung biomolekularer Hightech-Wirkstoffe, der sogenannten Biologika, hat die Therapie der Psoriasis revolutioniert. Eine hocheffektive und – abgesehen von geringen unerwünschten Arzneimittelwirkungen – langjährige Anwendung führt zumeist zu vollständiger oder nahezu vollständiger Abheilung zuvor ausgeprägter Befunde. So genügt beispielsweise eine vierteljährliche subkutane Injektion von Tildrakizumab in der Erhaltungstherapie (ILUMETRI®), einem monoklonalen IL23-Inhibitor, um diese Effekte zu erzielen. Und das Arsenal der Biologika und ihrer Surrogatwirkstoffe, der sogenannten Biosimilars, umfasst inzwischen über 30 Präparate verschiedenster namhafter Hersteller. Das in praxi limitierende Moment sind die sehr hohen, bis im fünfstelligen Bereich liegenden Jahreskosten. Selbst in vielen dermatologischen Praxen erfolgt die Verordnung eher zurückhaltend aus Rücksicht auf eventuelle Plausibilitätsprüfungen. So stellen Biologika gegen Psoriasis in der Hausarztpraxis eher keine praktikable Behandlungsoption dar.
Praxistipp:
Bezüglich der Verordnung von Biologika bei Psoriasis empfiehlt sich schon aus kassenrechtlichen Gründen die Überweisung zur Fachärztin bzw. zum Facharzt für Dermatologie.
Klassische Systemtherapie
Auch die UV-Therapie in Form von UV-B-311-nm-Schmalband oder PUVA-Bad (Metoxypsoralen lokal und UV-A-Bestrahlung) gilt als Systembehandlung. Der logistische Aufwand, die Verfügbarkeit, die begrenzte Effektivität, das Nebenwirkungspotenzial und das Arsenal an effektiveren Behandlungen stellen diese Behandlungsmethode zunehmend auf den Prüfstand. Im Setting der Hausarztpraxis ist die Durchführung und auch Vermittlung von Lichttherapie eher schwierig.
Auf eine seit weit über 30 Jahren bestehende klinisch-praktische Langzeiterfahrung in Deutschland kann bei den Fumarsäureestern zurückgeblickt werden. Dimethylfumarat (DMF) ist in diesem Zusammenhang ein in Wirksamkeit und Verträglichkeit bewährter Wirkstoffklassiker. In der Indikation der Psoriasis ohne Gelenkbefall ist DMF für die systemische perorale First-Line-Therapie zugelassen. Unter Beachtung des einschleichenden Dosierschemas können die unerwünschten Arzneimittelwirkungen in Form von gastrointestinalen Tenesmen und Diarrhö sowie gelegentlicher Flush-Symptomatik minimiert oder vermieden werden. Das günstige Sicherheitsprofil von SKILARENCE® ist vor allem im Vergleich zu anderen konventionellen Systemantipsoriatika wie Methotrexat (MTX), Ciclosporin oder Retinoiden ersichtlich. Insbesondere ist die Anwendung bei einer Vielzahl von Komorbiditäten wie Diabetes, Hepatopathie oder Nephropathie unbedenklich. Blutbildkontrollen sind nur vierteljährlich* erforderlich und sollen hauptsächlich Leuko- und Lymphozytopenie ausschließen. Als Immunmodulator wirkt DMF antiinflammatorisch und antiproliferativ und wirkt darüber hinaus auch der verhängnisvollen Kaskade des „psoriatischen Marsches“ entgegen, indem es die Adiponektin-Spiegel erhöht und die Endothelfunktion verbessert. DMF ist ein weitaus kostengünstigeres Systemtherapeutikum, dessen initialer Einsatz auch in der Hausarztpraxis eine gute Option sein kann.
Der Phosphodiesterasehemmer Apremilast ist ein Wirkstoff, der in der frühen Behandlung der Psoriasis und der Psoriasisarthritis zum Einsatz kommt, allerdings auch sehr kostenintensiv ist und bezüglich der Effektivität hinter den Biologika zurückbleibt. Apremilast kann Depressionen verstärken. Methotrexat, ein Folsäureantagonist, ist ein klassisches und auch effektives First-Line-Medikament bei moderater und schwerer Psoriasis und vor allem bei Psoriasisarthritis. Es ist wöchentlich s.c. oder p. o. zu verabreichen und wirkt vor allem immunsuppressiv. Allerdings birgt die Anwendung von Methotrexat bei Adipositas, Diabetes und nicht alkoholischer Fettleber hohe Risiken, und regelmäßige Blutbild- und Leberwertkontrollen sind obligat. Der Einsatz in der Hausarztpraxis ist durchaus eine Option. Die Anwendung des Immunsuppressivums Ciclosporin ist bei bestehender Hypertonie, Dyslipidämie und Nephropathie nicht ratsam. Das Retinoid Acitretin kommt vor allem bei palmoplantarer Psoriasis und bei Psoriasis pustulosa zum Einsatz, Warnhinweise schränken die Anwendung bei Bluthochdruck, Fettstoffwechselstörung, Adipositas, Diabetes und Depression ein.
* Wenn die Lymphozytenzahl auf <1.000 Zellen/Mikroliter fällt, aber ≥700 Zellen/Mikroliter ist, sollten die Blutwerte monatlich kontrolliert werden. Wenn die Lymphozytenzahl auf unter 700 Zellen/Mikroliter fällt, muss die Blutuntersuchung wiederholt werden. Wenn sich dabei bestätigt, dass der Wert unter 700 Zellen/Mikroliter liegt, muss die Behandlung sofort abgebrochen werden. Wenn die Leukozytenzahl auf <3.000 Zellen/Mikroliter fällt, sollte die Therapie mit SKILARENCE® abgebrochen werden.
Praxistipp:
Vor dem Hintergrund akzeptabler Wirksamkeit, guter Praktikabilität und überschaubarer Medikamentenkosten sind Dimethylfumarat und Methotrexat gute Optionen als First-Line-Antipsoriatika.
Lokale Initialtherapie und Erhaltungstherapie
Geht es um die Lokalbehandlung der Schuppenflechte, dann sind drei Behandlungsgrundsätze und dementsprechende Agenziengruppen zu unterscheiden.
Keratolytika sind in der Anfangsbehandlung bewährt. Ihre Aufgabe ist es, die teils sehr ausgeprägte Schuppung zu entfernen und damit einen besseren Angriff der antiinflammatorischen und antiproliferativen Wirkstoffe zu ermöglichen. Salicylsäure in unterschiedlicher Konzentration (in der Regel 5–20%) in Vaseline kann innerhalb weniger Tage ein beachtliches „Peeling“ erzielen. Es empfiehlt sich, die Behandlung der betroffenen Hautregionen über Nacht durchzuführen und die Salbenreste am nächsten Morgen abzuduschen. Salicylsäure löst Eiweiße auf und erhöht die Wasserbindungskapazität der Haut. Sie wirkt außerdem gegen Pilze und Bakterien. Carbamid (Synonyme: Urea, Harnstoff) ist vorwiegend ein „moisturizer“, d. h., es speichert Feuchtigkeit in der Haut über Ausbildung von Hydrathöhlen und ist in 5%iger Konzentration eher als Bestandteil von pflegenden Externa bekannt. In höheren Konzentrationen (10–20%) wirkt Carbamid aber auch keratolytisch.
Praxistipp:
Zu Beginn einer Psoriasisbehandlung bewährt sich eine Lokalbehandlung mit Salicylvaseline über drei bis fünf Nächte.
Entscheidendes lokales antipsoriatisches Prinzip ist die antiinflammatorische und antiproliferative Wirkung. Als lokaltherapeutischer Goldstandard gilt die Fixkombination aus dem Klasse-III-Steroid Betamethason und dem Vitamin-D-Derivat Calcipotriol. Das Steroid bekämpft die Entzündung, das Infiltrat und den Juckreiz und bewirkt eine Wiederherstellung der Hautbarriere, während das Vitamin-D3-Analogon Calcipotriol über selektiven Angriff an den Vitamin-D-Rezeptoren der Schuppenbildung und den Entzündungsreizen entgegenwirkt sowie das Zellwachstum normalisiert. Die wichtigsten Wirkungen sind die Proliferationshemmung und die Verbesserung der Keratinozytendifferenzierung. Als lokaltherapeutischer Goldstandard gilt die Fixkombination aus beiden Substanzen. Die Kombination hat drei entscheidende Vorteile. Erstens vereinfacht sie grundsätzlich die Anwendung. Zweitens ergänzen sich die Agenzien in ihrer Wirksamkeit synergistisch. Und drittens reduzieren sich die wechselseitigen unerwünschten Arzneimittelwirkungen, insbesondere der Atrophieeffekt des Steroids, sodass auch eine mehrwöchige Behandlung möglich ist [5, 6]. Die Fixkombination aus Betamethason und Calcipotriol kann indikationsgerecht (ICD-10-Code Psoriasis: L40.0 bis L40.9) grundsätzlich zulasten der gesetzlichen Krankenversicherung (GKV) verordnet werden.
Mit der Zielsetzung der weitestgehenden Erscheinungsfreiheit erfolgt initial eine einmal tägliche Anwendung bis zum Therapieerfolg, zumindest aber über 4–8 Wochen. In der nachfolgenden Erhaltungstherapie ist eine zweimal wöchentliche Anwendung der Fixkombination aus Betamethason und Calcipotriol angeraten. Prinzip ist hier eine proaktive Therapie, ähnlich wie bei der Anwendung der Calcineurininhibitoren bei der atopischen Dermatitis [7]. Zwischenzeitlich sollte der Effekt einer eingeleiteten Lokaltherapie überprüft werden [4]. Die Anwendung von Calcipotriol ist nach Fachindikation auf maximal 15–35% der Körperoberfläche zugelassen. Demnach sind bei Einhaltung der Grenzen keine relevanten Störungen des Kalziumstoffwechsels zu erwarten [8]. Hyperkalzämien sind nur in Einzelfällen infolge längerfristiger Überschreitungen der Höchstmengen beobachtet worden. Calcipotriol ist auch als Monotherapeutikum verfügbar, zeigt dann aber eine weitaus geringere Wirkung.
Praxistipp:
Goldstandard in der Lokaltherapie ist die Fixkombination aus dem Klasse-III-Steroid Betamethason und dem Vitamin-D3-Analogon Calcipotriol.
Monotherapeutische Klasse-III- und Klasse-IV-Steroide (z. B. Betamethason bzw. Clobetasol) sollten wegen der unerwünschten Steroidwirkungen nur wenige Tage (Gesicht, Intertrigines)* bis wenige Wochen (übriger Körper, Extremitäten) angewandt werden. Die unerwünschten Wirkungen der Steroide sind ebenfalls Folge der entzündungshemmenden, immunsuppressiven und antiproliferativen Hauptwirkungen (Hautatrophie, Teleangiektasien, Hautvulnerabilität, Pigmentverschiebungen). Das Klasse-III-Steroid Mometason gilt als Monosteroid mit dem vergleichsweise günstigsten therapeutischen Index (TIX), d. h. der Relation von Wirkung zu Nebenwirkungen. Es hat ein vernachlässigbar geringes Allergisierungspotenzial und eine vergleichsweise geringe systemische Resorptionsrate.
Nach anfänglicher monotherapeutischer Steroidtherapie wird gelegentlich auf die Calcineurininhibitoren (CNI) Pimecrolimus oder Tacrolimus gewechselt. Diese sind allerdings für die Therapie der Psoriasis nicht zugelassen, daher handelt es sich um eine „Off-label“-Behandlung. Bei nachweislicher Wirksamkeit in den typischen Manifestationen unter Folienokklusion bleibt die nicht okklusive Anwendung ohne signifikanten Effekt [9, 10]. In Ermangelung zugelassener Alternativen wird die Behandlung gelegentlich erfolgreich in Problemregionen wie Gesicht, Intertrigines und Genito-Anal-Bereich angewandt. Calcineurininhibitoren beeinflussen immunmodulatorisch die Aktivierung sowohl von T-Zellen als auch von Keratinozyten und Mastzellen [4].
Schließlich komplettiert die wirkstofffreie Basistherapie die Lokalbehandlung der Psoriasis. Sie dient der Rückfettung, deren Grad durch die Creme- oder Salbengrundlage ausgewählt werden kann.
Etwa 50% der Patientinnen und Patienten zeigen eine leichte Ausprägung der Psoriasis und können ausschließlich lokaltherapeutisch behandelt werden [11]. Etwa 90% der an Psoriasis Erkrankten verwenden topische Therapeutika. In der aktuellen S3-Leitlinie zur Therapie der Psoriasis wurden in Ermangelung neu zugelassener topischer Antipsoriatika fast ausschließlich die systemischen Therapieempfehlungen umfassend angepasst. Daher folgen die hier dargelegten Lokaltherapieprinzipien im Wesentlichen den Empfehlungen der PsoNet-Sprecherkonferenz und der Nationalen Versorgungskonferenz Psoriasis.
Die Patientenakzeptanz der topischen Behandlung der Psoriasis
Obwohl wirksam, etabliert, empfohlen und sicherer im Vergleich zur Systemtherapie findet die Lokaltherapie der Psoriasis nicht immer die notwendige Akzeptanz seitens der betroffenen Patienten. Patientenadhärenz aber stellt eine ganz wesentliche Voraussetzung für die erfolgreiche Behandlung chronischer Hauterkrankungen dar.
Der Therapieerfolg mit einem Externum hängt nicht ausschließlich von der Effektivität des applizierten Wirkstoffs ab, denn die Patiententreue ist stark verknüpft mit den Vehikeleigenschaften und der zugrunde liegenden Galenik. Erfahrungsgemäß ist es ungünstig, wenn das Externum sehr fettig auf der Haut liegt, wenn es nur langsam in die Haut einzieht und in einer zeitraubenden Salbungsprozedur resultiert. Auch Färbeeffekte an Textilien sind problematisch. Die Folge sind Therapieuntreue oder gar Therapieabbruch. Deutlich wurde diese Problematik im Zusammenhang mit der Fixkombination aus Betamethason und Calcipotriol. Hauptsächlich aufgrund von pH-Instabilität lassen sich beide Wirkstoffe extrem schlecht in wässrige Grundlage bringen. Lange Zeit waren die handelsüblichen Präparate nur als Salben oder Schaumdispersionen von ölig-fettiger Konsistenz verfügbar, die von vielen Patientinnen und Patienten nicht lange genug angewandt oder gar abgelehnt wurden. Inzwischen jedoch ist es mittels einer neuartigen Technologie gelungen, die Fixkombination aus Betamethason und Calcipotriol in eine wasserhaltige Cremeformulierung (stabile Öl-in-Wasser-Emulsion) zu bringen.
Mithilfe dieser sogenannten PAD-Technologie (Poly-Aphron-Dispersion) sind Betamethason und Calcipotriol in separate multimolekulare Schichten von Emulgatorhüllen eingeschlossen, sodass beide Wirkstoffe stabil in der wasserhaltigen Grundlage vorliegen. Erst beim Auftragen und Verreiben der Creme auf der Haut werden die Stoffe nach dem Aufbrechen dieser Emulgatorhüllen freigesetzt. Seit Oktober 2021 ist WYNZORA® Creme in der Europäischen Union für die Lokalbehandlung der leichten und mittelschweren Plaque-Psoriasis einschließlich der Kopfhautpsoriasis zugelassen. Die gute Verträglichkeit, ein hoher Behandlungskomfort und vor allem eine hohe Patientenakzeptanz sowie Verbesserung der Lebensqualität sind in diversen Studien bestätigt worden [12]*. Das bewährte Wirkstoffkonzept in innovativer Galenik hat das Potenzial, eine Rückbesinnung auf die Vorteile der antipsoriatischen Lokaltherapie zu induzieren. Die wässrige Creme hat nachweislich eine gute Wirksamkeit und ein vorteilhaftes Sicherheitsprofil, sie zieht schnell ein und wird von den Patientinnen und Patienten als angenehm empfunden.
Bei der Psoriasis leichten Schweregrades wird die alleinige Lokaltherapie mit der Fixkombination aus Betamethason und Calcipotriol den Empfehlungen der Leitlinien gerecht. Gerade die Plaque-Psoriasis der Extremitäten kann effektiv und unkompliziert behandelt werden. Die Wahl der geeigneten Galenik kann die Therapietreue der Behandelten eher positiv beeinflussen (Abb. 14).
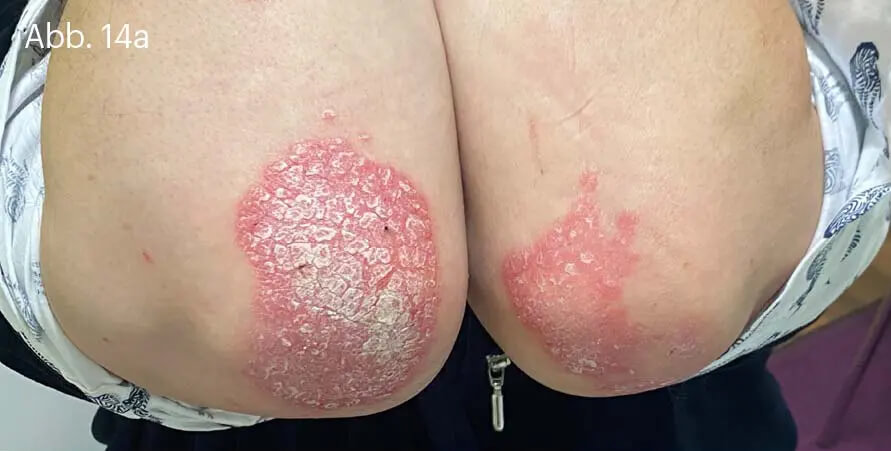
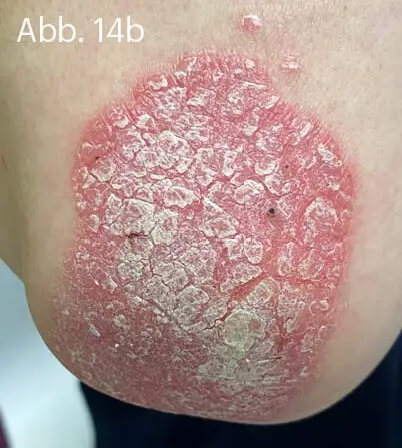
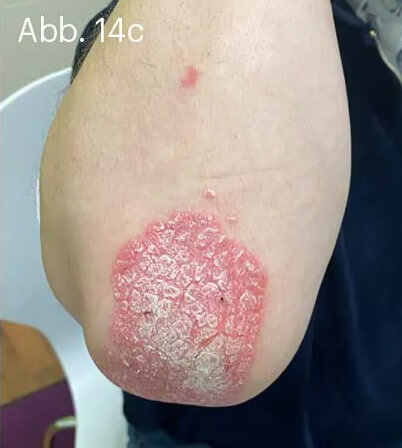



Abb. 14: 54-jähriger Patient mit langjährig bestehender Plaque-Psoriasis der Ellenbogen. Hier finden sich scharf begrenzte, bis 10 cm durchmessende, erythrosquamöse Plaques (a) mit mittel- bis groblamellärer Schuppung (b). Daneben sind einzelne kleinere Satellitenläsionen sichtbar (c).
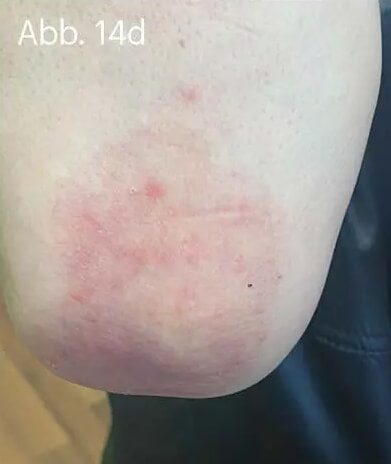
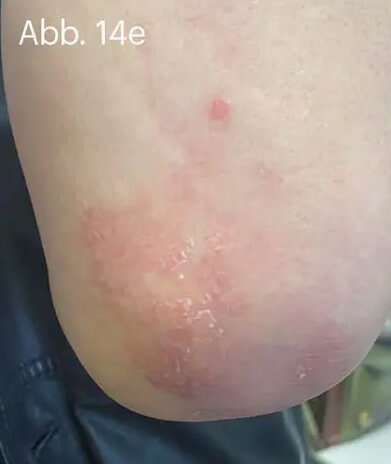
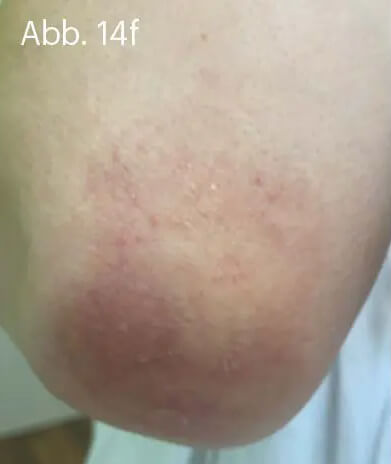
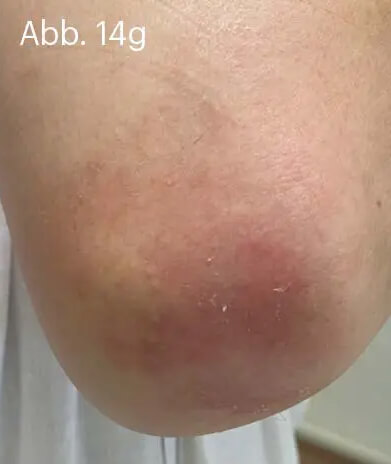
Abb. 14: Unter topischer Anwendung von WYNZORA® Creme waren im Verlauf von zwei (d, e) bis drei Wochen (f, g) die Plaques bis auf residuale Erytheme nahezu abgeheilt. Voraussetzung für den Therapieerfolg war die kontinuierliche tägliche Anwendung der WYNZORA® Creme. Anamnestisch konnte eruiert werden, dass vorangegangene Lokaltherapien mit den gleichen Wirkstoffen in stark rückfettender Galenik vom Patienten schlecht toleriert und daher nach kürzerer Zeit abgebrochen worden waren. Im weiteren Verlauf wurde die Behandlung auf eine Monotherapie mit Calcipotriol umgestellt. Es konnte ein dauerhaft zufriedenstellendes Therapieergebnis langfristig erhalten werden.
Praxistipp:
Gut verträgliche Galenik eines Externums ist Voraussetzung für Patientenadhärenz und Therapieerfolg. WYNZORA® Creme enthält Betamethason und Calcipotriol in wasserhaltiger Galenik auf Basis der PAD-Technologie und ist verschreibungsfähig nach GKV.
*Siehe Beschreibung der weiteren explorativen Endpunkte DLQI aus zwei prüfarztverblindeten klinischen Studien in der gepoolten Analyse von Pinter A, Green LJ, Selmer J et al. A pooled analysis of randomized, controlled, phase 3 trials investigating the efficacy and safety of a novel, fixed dose calcipotriene and betamethasone dipropionate cream for the topical treatment of plaque psoriasis. J Eur Acad Dermatol Venereol. 2022 Feb;36(2):228–236. doi: 10.1111/jdv.17734.: “The mean DLQI improvement from baseline, at Week 8, was significantly greater for CAL/BDP PAD-cream (6.5 points) compared to CAL/BDP TS (5.6 points, p < 0.0001) and vehicle (2.5 points, p < 0.0001).” Bei dem weiteren explorativen Endpunkt handelt es sich weder um einen primären noch um einen sekundären Endpunkt. Daten zur Psoriasis der Kopfhaut wurden in der gepoolten Analyse nicht berücksichtigt.
Lokaltherapie bei Problemlokalisationen und in Schwangerschaft und Stillzeit
Bei Manifestation in den Körperfalten, genitoanal und an der Gesichtshaut ist die einmal tägliche Anwendung von Steroiden der Stärkeklassen II und III indiziert. Nach Therapieansprechen innerhalb von zwei Wochen kann die Behandlung „off-label“ mit topischen Calcineurininhibitoren weitergeführt werden, insbesondere zur Vermeidung von Steroidnebenwirkungen. Die Wirkung von Tacrolimus oder Pimecrolimus in diesen Problemlokalisationen ist in kleineren Studien belegt [13, 14]. Wenngleich die Kombination aus Betamethason und Calcipotriol nicht direkt für die Anwendung in den Intertrigines zugelassen ist, so wird sie in Ermangelung wirksamer Alternativen in praxi über begrenzte Zeit doch erfolgreich durchgeführt, zumal die hier behandelte Fläche relativ klein ist. Psoriasis palmoplantaris und Psoriasis capillitii sind zumeist stark entzündliche Manifestationen der Psoriasis, die funktionell stark hinderlich bzw. kosmetisch extrem belastend sind. Hier empfiehlt sich bei starker Schuppung in jedem Falle die Keratolyse mit Salicylvaseline. Vorübergehend kann auch eine Initialbehandlung mit Klasse-IV-Steroiden als Creme bzw. Lösung oder Schaum appliziert werden. Inzwischen bestehen hervorragende Praxiserfahrungen in beiden Lokalisationen mit WYNZORA® Creme (Abb. 15).

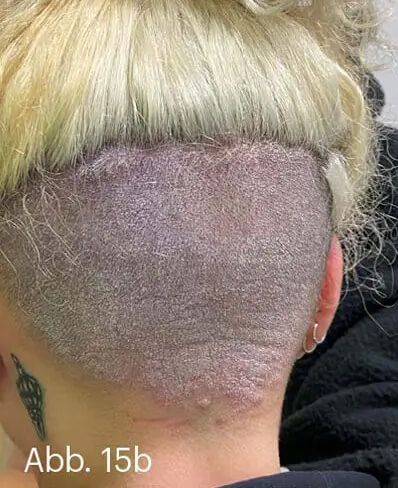
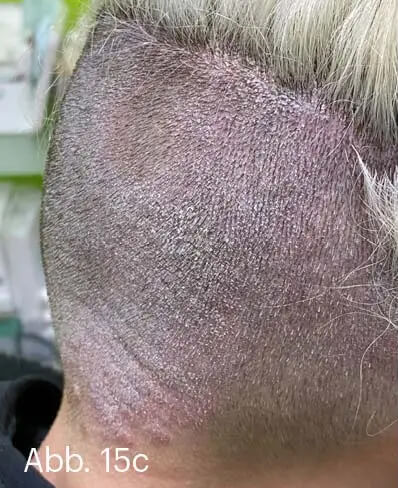
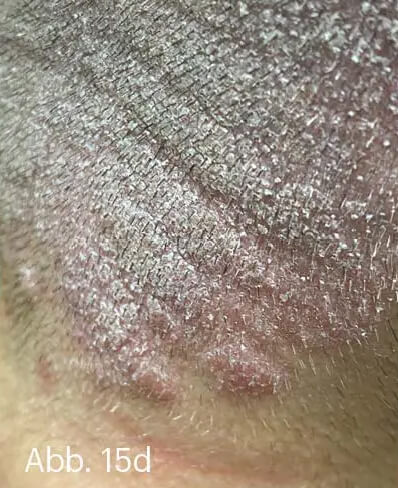
Abb. 15: 32-jährige Patientin mit ausgeprägter Psoriasis capitis. Wegen Kinderwunsches hatte sie eine Systemtherapie grundsätzlich abgelehnt. Monotherapien mit Steroidschäumen und Calcipotriol-haltigen Gelen hätten keinen nachhaltigen Effekt gehabt. Kombinationspräparate hätten bessere Wirkung gezeigt, wären aber wegen der stark rückfettenden Galenik im Bereich des behaarten Kopfes nicht dauerhaft praktikabel gewesen. Zuletzt war die Patientin dazu übergegangen, das Kopfhaar über den betroffenen Kopfhautstellen abzurasieren. Im Bereich des unter dem deckenden Haupthaar (a) nahezu kahl rasierten hinteren Kapillitiums (b) zeigte sich eine fein- bis mittellamellär schuppende, flächig-homogene, entzündliche Plaque (c) mit insbesondere okzipital ausgeprägtem entzündlichen Infiltrat (d).


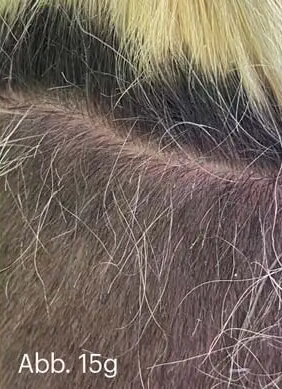
Abb. 15: Nach Anwendung der von der Patientin wesentlich besser tolerierten WYNZORA® Creme war bereits nach vier Wochen eine nahezu vollständige Rückbildung der entzündlichen Plaques zu sehen (e–g). Zu ihren Erfahrungen befragt, erklärte die Patientin, dass die WYNZORA® Creme unproblematisch aufzutragen gewesen und rasch und angenehm eingezogen sei. Färbeeffekte hätte sie weder an den Textilien noch im Haupthaar bemerkt.
Fazit
Die Hausarztpraxis wird oft und zumeist primär mit dem Krankheitsbild der Schuppenflechte konfrontiert. Vor dem Hintergrund der Diskrepanz zwischen der Vielzahl an Patientinnen und Patienten und der begrenzten dermatologisch-fachärztlichen Kapazitäten ist das aktive diagnostische und therapeutische Handeln der allgemeinmedizinischen und internistischen Hausärztinnen und Hausärzte unverzichtbar. Wichtig ist die Unterscheidung zwischen leichter und moderater bzw. schwerer Psoriasis. Etwa die Hälfte aller Betroffenen kann aufgrund der leichten Ausprägung der Erkrankung mittels Initialtherapie und Erhaltungstherapie mit der Fixkombination aus Calcipotriol und Betamethason leitliniengerecht und entsprechend den Vorgaben der gesetzlichen Krankenversicherung behandelt werden. Eine neuartige Galenik dieser Fixkombination als wasserhaltige Creme mit PAD-Technologie bietet die Chance auf größere Patientenakzeptanz und damit auch verbesserte Patientenadhärenz als Voraussetzung für den Therapieerfolg. Nach Ermessen und Erfahrung kann in der Hausarztpraxis prinzipiell auch systemisch therapiert werden. Für den Einsatz von Biologika ist grundsätzlich die Überweisung zur Fachärztin bzw. zum Facharzt für Dermatologie empfohlen.
Weitere Informationen
WYNZORA®

WYNZORA®
50 Mikrogramm/g + 0,5 mg/g Creme
Zugelassene Indikation:
Zur topischen Behandlung einer leichten bis mittelschweren Psoriasis vulgaris (einschließlich Psoriasis der Kopfhaut) bei Erwachsenen.
Wirkstoffe:
1 g Creme enthält 50 Mikrogramm Calcipotriol und Betamethasondipropionat entsprechend 0,5 mg Betamethason.
- Czaika et al: Entzündliche Dermatosen. In: Kurzlehrbuch Dermatologie – entzündliche Dermatosen, 3. Aufl. 2023, S. 133–139, Georg Thieme Verlag Stuttgart.
- Mrowietz, U., Prinz, J.C. (2018). Psoriasis. In: Plewig, G., Ruzicka, T., Kaufmann, R., Hertl, M. (eds) Braun-Falco’s Dermatologie, Venerologie und Allergologie. Springer Reference Medizin. Springer, Berlin, Heidelberg.
- Nast A, et al. S3-Leitlinie: Therapie der Psoriasis vulgaris. AWMF-Reg.-Nr. 013–001; 2021.
- Körber A, et al. Topische Therapie bei Psoriasis vulgaris – ein Behandlungspfad. J Dtsch Dermatol Ges. 2019;17(Suppl4):3–14.
- Kragballe K, et al. Calcipotriol cream with or without concurrent topical corticosteroid in psoriasis: tolerability and efficacy. Br J Dermatol. 1998;139(4):649–54.
- Ruzicka T, Lorenz B. Comparison of calcipotriol monotherapy and a combination of calcipotriol and betamethasone valerate after 2 weeks’ treatment with calcipotriol in the topical therapy of psoriasis vulgaris: a multicentre, double-blind, randomized study. Br J Dermatol. 1998;138(2):254–8.
- Neri L, Miracapillo A. Treatment adherence and real-lifeeffectiveness of topical therapy in patients with mild or moderate psoriasis: uptake of scientific evidence in clinical practice and dermatologists’ preferences for alternativetreatment options. G Ital Dermatol Venereol. 2015;150(1):19–26.
- Wilsmann-Theis D, Gerdes S, Körber A, et al. Topische Therapie der Psoriasis. 1. Aufl. Bremen: UNI-MED, 2016.
- Mrowietz U, et al. The novel ascomycin derivative SDZ ASM 981 is effective for psoriasis when used topically under occlusion. Br J Dermatol. 1998;139(6):992–6.
- Remitz A, et al. Tacrolimus ointment improves psoriasis in a microplaque assay. Br J Dermatol. 1999;141(1):103–7.
- Langenbruch A, et al. Quality of Psoriasis care in Germany: results of national health care study „PsoHealth3“. Arch Dermatol Res. 2016;308(6):401–8.
- Pinter A, et al. A pooled analysis of randomized, controlled, phase 3 trials investigating the efficacy and safety of a novel, fixed dose calcipotriene and betamethasone dipropionate cream for the topical treatment of plaque psoriasis. J Eur Acad Dermatol Venereol. 2022;36(2):228–36.
- Lebwohl M, et al. Proven efficacy of tacrolimus for facial and intertriginous psoriasis. Arch Dermatol. 2005;141(9):1154.
- Lebwohl M et al. Tacrolimus ointment is effective for facial and intertriginous psoriasis. J Am Acad Dermatol. 2004;51(5):723–30.
- Semenov YR, et al. Psoriasis and mortality in the United States: data from the National Health and Nutrition Examination Survey. J Am Acad Dermatol. 2021;85(2):396–403.
- Mrowietz U, et al. Definition of treatment goals for moderate to severe Psoriasis: a European consensus. Arch Dermatol Res. 2011;303(1):1–10.
- Koehm M, et al. Predictive value of different tools for detection of psoriatic arthritis in patients with psoriasis in daily routine care using questionnaires for diagnosis of psoriatic arthritis and fluorescence-optical imaging technique. Arthritis Rheumatol. 2016;68(Suppl10):2158–9.
- Ibrahim GH, et al. Evaluation of an existing screening tool for psoriatic arthritis in people with psoriasis and the development of a new instrument: the Psoriasis Epidemiology Screening Tool (PEST) questionnaire. Clin Exp Rheumatol. 2009;27:469–74.
- Boehnke W-H, Boehncke S, Tobin A-M, Kirby B: The ‚psoriatic march‘: a concept of how severe psoriasis may drive cardiovascular comorbidity. Exp Dermatol 2011 Apr;20(4):303–7.
- Augustin M, et al. Co-morbidity and age-related prevalence of psoriasis: analysis of health insurance data in Germany. Acta Derm Venereol. 2010;90(2):147–51.
- Armstrong AW, et al. Quality of life and work productivity impairment among psoriasis patients: findings from the National Psoriasis Foundation survey data 2003–2011. PLoS One. 2012;7(12):e52935.
- Langley RG, et al. Psoriasis: epidemiology, clinical features, and quality of life. Ann Rheum Dis. 2005;64(Suppl2):ii18–23.
- Kolios AG, et al. Swiss S1 guidelines on the systemic treatment of psoriasis vulgaris. Dermatology. 2016;232(4):385–406.